바이러스가 사람의 세포 속으로 들어갈 때 중요한 역할을 하고 있는 것이 스파이크 단백질이다.
껍질에 배열돼 있는 돌기상(突起狀) 구조물인데 길이는 10~15nm로 세포막에 있는 단백질 수용체와 결합해 우리 몸에 침투하는 일을 전담하고 있다.
그동안 과학자들은 이 스파이크(spike)를 표적으로 다양한 연구를 진행해왔다. 그리고 2002년 발생한 사스(SARS)는 우리 몸의 단백질 수용체인 ‘ACE2’를, HIV나 에볼라는 단백질을 활성화시키는 효소 ‘퓨린(furin)’을 표적으로 삼는다는 사실을 알아냈다.
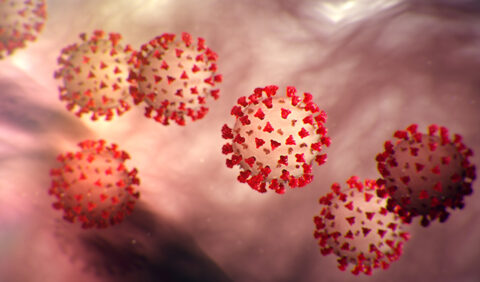
스파이크 유전자 서열 사람 세포와 유사
2일 ‘뉴사이언티스트’에 따르면 처음에 과학자들은 코로나19를 유발하는 신종 바이러스(SARS-CoV-2)의 유전자 구조가 동종 계열인 사스와 비슷할 것으로 판단해왔다.
그러나 지난 3월 프랑스, 중국 등의 과학자들이 새로운 사실을 밝혀냈다. 신종 바이러스가 HIV‧에볼라 바이러스처럼 ‘퓨린’을 타깃으로 삼고 있다는 것. 스파이크 단백질 안에 ‘퓨린’과 유사한 분절 부위(furin-like cleavage site)가 있다는 사실을 발견했다.
과학자들은 ‘퓨린’이 폐, 간, 소장 등 많은 장기 내 조직에서 발견되므로, 스파이크가 인체 세포에 침투할 경우 여러 조직을 공격할 수 있으며, 이런 사실을 근거로 프랑스 엑스마르세유 대학 연구팀은 “사스보다 100배에서 1000배 더 빠르게 전파될 수 있다.”는 주장을 편 바 있다.
단백질분해효소(protease)인 퓨린은 단백질을 이루고 있는 아미노산 간의 펩티드 결합을 가수분해하는 효소다.
섭취하는 단백질을 분해해 다양한 역할을 담당할 수 있도록 매개체 역할을 하는데 문제는 바이러스에게도 같은 역할을 한다는 것이다. 바이러스가 침투하면 바이러스 유전체에서 발현되는 단백질을 여러 조각으로 잘라 다양한 기능을 수행할 수 있는 또 다른 바이러스를 만들어낸다.
그동안 과학자들은 신종 바이러스(SARS-CoV-2)의 스파이크 단백질 속에 있는 이 ‘퓨린’과 유사한 분절 부위를 통해 사람 세포에 있는 ‘퓨린’에 침투하고 있으며, 침투 후 스파이크 단백질이 2개로 분리된다는 결론에 도달하고 있었다.
그리고 지난 3월 26일 국제공동연구팀은 스파이크 단백질 속에 있는 이 ‘퓨린’과 유사한 분절 부위의 유전자 서열이 사람의 ‘상피 세포 나트륨 통로(epithelial sodium channel)’의 유전자 서열과 일치한다는 연구 결과를 발표한 바 있다.
스파이크 통제하면 신속 치료 가능해져
상피 세로란 몸의 표면이나 내장기관의 내부 표면을 덮고 있는 세포로 몸을 보호하는 역할을 맡고 있다.
내부를 보호하기 위해 세포간 물질이 적고 세포가 촘촘하게 늘어서 있는 모습을 보인다. 유전자 서열이 같다는 것은 신종 바이러스(SARS-CoV-2)가 사람 몸에 손쉽게 침투하고 있음을 말해주는 것이다.
이 같은 발견에 주목한 생명공학을 위한 인공지능업체 엔퍼런스(nference)에서는 곧 연구에 착수했다.
그리고 세계 전역에서 수집한 신종 바이러스의 스파이크 단백질을 분석한 결과 1만 967개 중 1만 956개에서 4개의 아미노산으로 구성돼 있는 공통 구조가 존재한다는 연구결과를 발표한다. 이전의 박쥐, 천산갑 등에서 발견한 바이러스에게서는 볼 수 없었던 구조였다.
그동안 베일에 가려져 있던 스파이크 단백질에 대한 의문이 밝혀지면서 엔퍼런스의 과학자들은 코로나19에 감염된 환자와 그렇지 않은 사람들, 그리고 원숭이, 쥐와 같은 동물들을 비교해가면서 유전자 검사를 이어나갔다.
그리고 스파이크 단백질 속의 ‘퓨린’과 유사한 분절 부위의 유전자 서열이 사람의 ‘상피 세포 나트륨 통로’는 물론 사스(SARS)의 단백질 수용체였던 ‘ACE2’와도 겹치는 부분이 있다는 새로운 사실을 확인하고 있다.
엔퍼런스의 연구책임자인 벵키 순다라라리안(Venky Soundararajan) 박사는 퓨린과 퓨린이 발견되는 다수의 장기들, 숙주세포 내 단백질 수용체인 ACE2와 호흡기, 사람의 상피 세포 나트륨에 이르기까지 총체적으로 신종 바이러스 침투의 통로가 되고 있다고 설명하고 있다.
그동안 코로나19가 다른 바이러스들과 달리 빠르고 광범위하게 확산되고 있는 이유를 어느 정도 말해주고 있는 대목이다.
엔퍼런스 연구결과와 관련 우려도 제기되고 있다.
미국 해컨색 메리디언 헬스센터의 연구책임자 데이비드 페를린(David Perlin) 박사는 “아직까지 학회 등을 통해 검증되지 않은 연구 결과를 성급하게 발표할 때 조심해야 할 부분이 있다.”고 말했다.
그러나 스파이크 단백질의 활동을 통제하는 일은 향후 백신 및 치료제 개발과 직결되는 일이다.
과학자들에 의해 신종 바이러스의 스파이크 단백질에 대해 그동안 몰랐던 사실들이 하나둘 밝혀지면서 백신 개발은 물론 새로운 치료제 개발에 한발 다가서고 있는 중이다. 백신과 치료제 개발을 고대하는 사람들에게 벅찬 기대감을 심어주고 있다.
- 이강봉 객원기자
- aacc409@hanmail.net
- 저작권자 2020-06-05 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터