같은 암 진단을 받고 비슷한 시기에 같은 약을 처방받아도 치료 결과가 사람마다 다르게 나오는 일은 드물지 않았다. 새로운 항암제가 개발되어 일부 환자에게서는 뚜렷한 효과를 보이기도 하지만, 다른 환자에게는 기대만큼 효과가 나타나지 않거나 얼마 지나지 않아 내성이 생기기도 한다. 항암 치료 기술이 발전할수록 좋은 약을 찾는 일 못지않게 그 약이 누구에게, 또 왜 더 잘 듣는가를 이해하는 일이 중요해지는 이유이다.
같은 약이라도 효과가 같지 않은 이유
그동안 항암 치료 효과의 개인차는 종양 혈관 구조의 차이와 종양 미세환경의 이질성으로 인해, 약물이 환자마다 다르게 분포하고 작용하기 때문인 것으로 여겨졌다. 실제로 암 조직의 혈관은 정상 조직보다 훨씬 무질서하고 불균일하기 때문에 약물이 고르게 스며들지 못한다. 그런데 최근 네이처 커뮤니케이션스에 게재된 연구는 여기서 한 걸음 더 나아간 새로운 시각을 제시하였다. 항암제가 종양 조직 안으로 잘 들어간 후에도 모든 세포에 고르게 퍼지는지, 세포 안에서도 어디에 얼마나 쌓이는지가 치료 효과를 크게 바꿀 수 있다는 것이다.
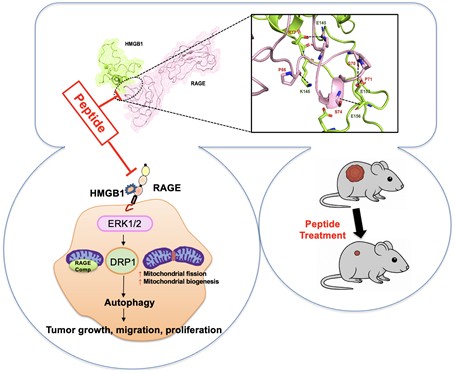
연구를 주도한 영국 MRC 의약 연구소의 페츠 박사는 난소암 치료에 사용되는 PARP 억제제가 환자별, 세포별로 균일하게 듣지 않는 이유를 추적하였다. PARP는 세포핵 안에서 DNA 손상을 감지하고 수리하도록 돕는 단백질이다. 암세포들은 원래 DNA가 불안정한 상태인데 이때 PARP까지 막아 버리면 암세포는 손상된 DNA를 더 이상 감당하지 못하고 죽게 된다. 이러한 원리를 이용하는 약이 바로 PARP 억제제인데, 이미 난소암 치료에서 중요한 약물군으로 사용되고 있으며 유방암과 전립선암 등 다른 암종에도 널리 쓰이거나 시험되고 있다.
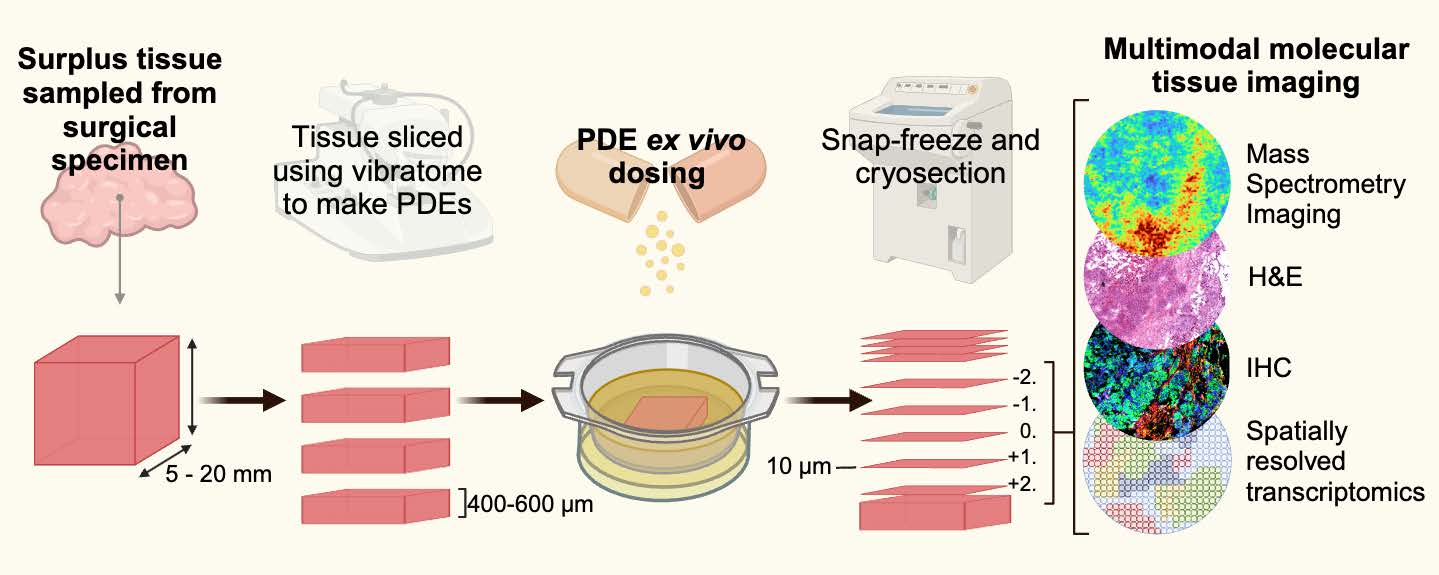
문제는 이 약물이 이론적으로는 잘 들어맞는 듯 보여도, 실제 환자에서는 반응 차이가 크다는 점이다. 연구진은 그 원인을 찾기 위해 난소암 환자의 조직을 수술로 제거한 후 얇은 슬라이스(수백 마이크로미터)로 잘라 배양액 속에서 살아 있는 상태를 유지하였다. 이를 엑스플란트(explant) 모델이라고 하는데, 이 방식의 가장 큰 장점은 실제 인간 종양의 3차원 미세구조가 유지된 상태에서 약물의 효과를 확인할 수 있다는 것이다. 연구진은 난소암 환자에게서 얻은 종양 조직으로 엑스플란트 모델을 만들고 PARP 억제제를 투여한 후 더 얇은 슬라이스(10 마이크로미터)로 나누어 질량 분석 이미징, 공간 전사체 분석, 면역 염색 등을 수행하였다. 종양 조직의 복잡성은 유지하면서 약물이 주로 어디에 분포하는지, 주변 세포는 어떤 상태였는지를 겹쳐서 해석하기 위한 일종의 ‘종합 검진 분석’ 전략인 것이다.
같은 암 조직에서도 세포마다 5배 약물 농도 차이
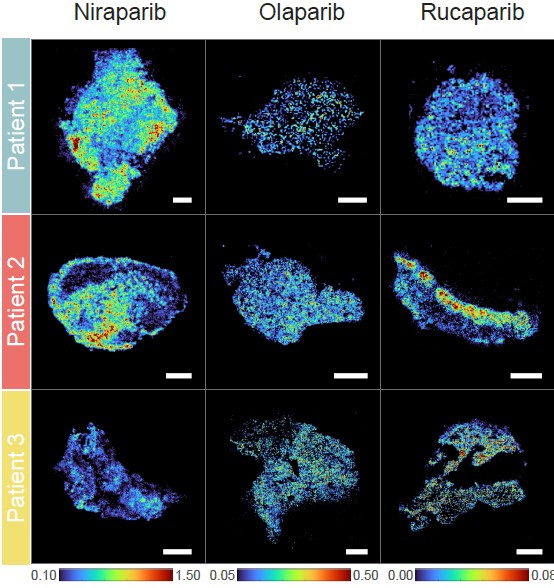
질량 분석 이미징을 통하여 확인한 결과는 예상보다 훨씬 불균일했다. 조직 내 어떤 부분에서는 약물이 진하게 몰려 있었던 반면 어떤 부분은 거의 보이지 않았는데, 같은 슬라이스 내부에서도 5배 이상 농도 차이를 보였다. 그렇다면 약물 고농도 구역의 세포와 저농도 구역의 세포는 어떤 차이가 있을까? 공간 전사체 분석을 통하여 알아본 결과, 약물이 많이 쌓인 구역의 세포일수록 세포 사멸과 DNA 손상 반응 유전자들이 더 높게 발현되어 있었다. 약물이 더 높게 축적된 곳에서 실제로 약효도 더 강하게 보였다는 뜻이니 이는 당연해 보일 수 있다.
흥미로운 점은 약물이 많이 축적된 구역의 세포에서 리소좀 관련 유전자들이 유난히 높게 측정된 것이다. 리소좀은 세포 안에서 노폐물과 고장 난 소기관을 분해하는 재활용 공장으로써, 산성이 강한 작은 주머니 모양의 구조이다. 리소좀과 약물 분포 사이의 연관성을 규명하기 위해 연구팀은 추가적인 세포 실험을 진행하였는데, 그 결과 리소좀 양이 많은 세포일수록 PARP 억제제가 더 많이 축적되어 있다가 서서히 방출되는 것을 확인하였다. 흔히 ‘세포의 쓰레기 처리장’으로 비유되는 리소좀이 항암 치료 측면에서는 ‘약물 저장고’ 역할을 하는 것이다. 리소좀으로 약물을 빨아들인 세포들 덕분에 주변 세포들은 약물에 상대적으로 덜 노출될 수 있었다. 같은 약을 써도 어떤 암세포는 쉽게 죽는 반면 다른 암세포는 이를 피하는 원인인 것이다.
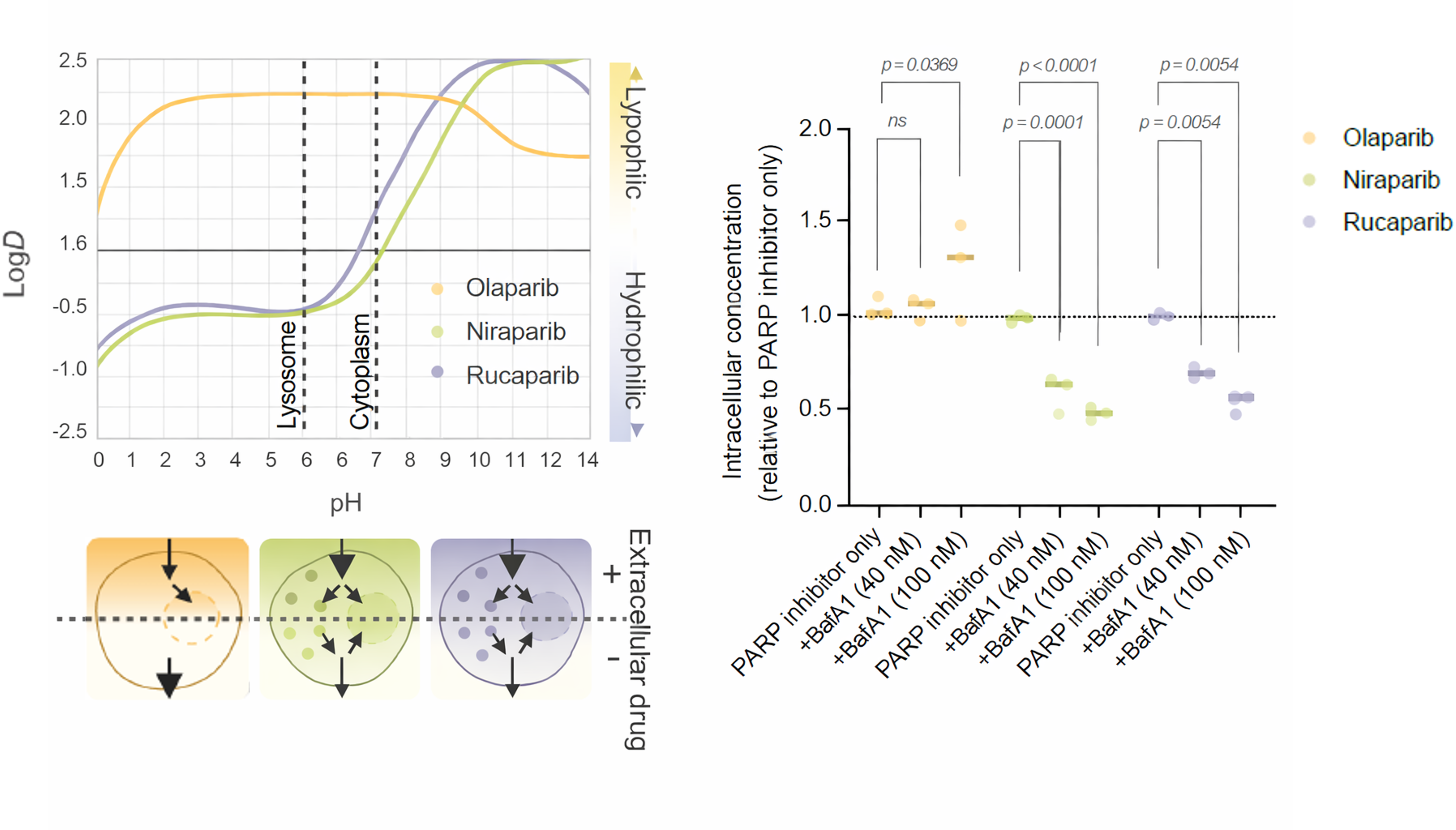
약물이 리소좀에 갇히게 된 이유도 확인되었다. 리소좀 내부는 산성이 강한데, 일부 약물 분자들은 이런 환경에서 양전하를 띠며 빠져나오기 어려워진다. PARP 억제제 중 루카파립과 니라파립은 이런 성질을 가진 약한 염기성 약물이라서 리소좀에 오래 갇혀있던 반면, 리소좀에 상대적으로 덜 축적되는 올라파립은 이러한 특성이 훨씬 적었다. 또한 리소좀의 산성도를 흐트러뜨리자 루카파립과 니라파립의 세포 내 농도는 줄어들었지만 올라파립은 거의 영향을 받지 않았다. 같은 계열의 약물이라도 세포 안에서 머무는 방식이 서로 다르며 그에 따른 치료 효과도 다를 수 있는 것이다.
세포의 재활용 공장이 약물 창고가 되다
이번 연구는 항암제의 성공 여부가 약물이 종양까지 도달했는지뿐만 아니라 종양 내부에서 어디로 스며들고, 세포 내부에서는 어떻게 처리되는지에 달려있을 수 있음을 보여준다. 같은 용량을 사용해도 어떤 세포는 충분한 양의 약물에 노출되지만 다른 세포는 그렇지 않을 수 있다. 종양 안에서도 일부 세포는 잘 죽고 일부 세포는 살아남는다면 결국 재발이나 내성의 씨앗이 될 가능성이 생긴다. 또한 이번 실험에 사용된 질량 분석 이미징과 공간 전사체 분석을 병합한 조직 분석 기술을 통하여 약물이 어떻게 퍼지는지, 어떤 유전자 특성을 가진 세포가 약물을 많이 흡수하는지 예측할 수 있었다. 이는 향후 개별 환자의 종양을 분석해 가장 적합한 약물을 선택하고 치료 전략을 세우는 데 도움이 될 것이다. 항암제의 미래는 더 강한 약을 만드는 일과 함께 약이 종양 속에서 어떤 여정을 거치는지 이해하는 일에 달려 있을지도 모른다.

관련 연구 바로 보러 가기
- 정회빈 리포터
- acochi@hanmail.net
- 저작권자 2026-04-24 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터