특정 유전자를 조작하여 질병을 치료하거나 특별한 능력은 얻는 이야기는 수많은 SF 소설과 영화의 단골 소재였다. 현실에서는 DNA를 손쉽게 수정할 수 있는 크리스퍼(CRISPR) 유전자 가위가 2012년 개발되고 이후 관련 기술들이 빠르게 발전하면서, 유전자 조작으로 질병에서 자유로운 미래를 실현시킬 수 있을 것이란 기대도 높아졌다. 하지만 실제 생물학은 영화 속 이야기보다 훨씬 복잡하다. 대부분의 질병은 하나의 유전자만으로 설명되지 않으며, 대부분의 경우 생활 습관과 환경, 여러 유전자의 상호작용이 얽혀 나타나는 경우가 훨씬 많기 때문이다.
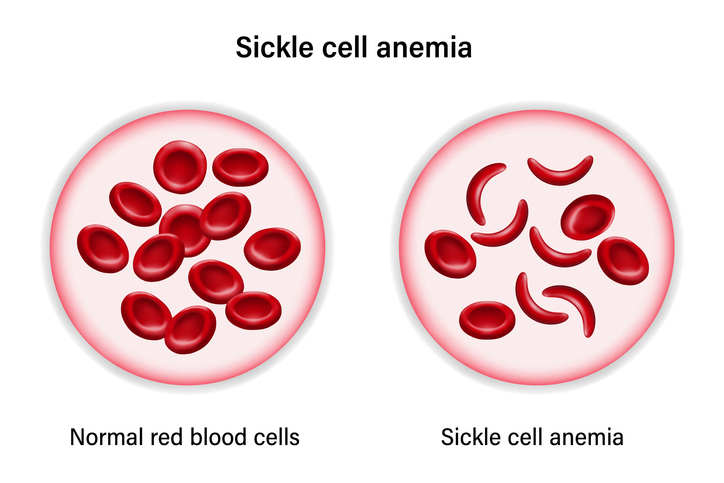
그럼에도 만약 하나의 유전자 변이만으로 발생하는 질병이 있다면 이런 질병은 유전자 가위 기술로 완전히 치료할 수 있지 않을까? 실제로 이러한 아이디어를 실현하여 2023년 미국 식품의약국(FDA)의 승인을 받은 치료제가 있는데 바로 카스제비(Casgevy)가 그것이다. 카스제비가 표적으로 삼는 질환은 겸상 적혈구 빈혈증(Sickle Cell Anemia)인데 헤모글로빈 유전자에 이상이 생겨 낫 모양의 비정상적인 적혈구가 만들어져 빈혈을 유발하는 질환이다. 카스제비는 CRISPR 기반 유전자 편집 기술을 사용하여 환자의 혈액 줄기세포 DNA를 체외에서 수정한 뒤 다시 체내로 주입하는 방식으로 치료 효과를 낸다. 이처럼 특정 유전자 변이를 직접 교정하는 방식의 치료 전략은 최근 유전 질환 연구에서 중요한 흐름으로 자리 잡고 있다.
유전자 교정만으로 병을 고칠 수 있을까
하나의 유전자를 고치는 것만으로도 질병을 치료하는 사례가 등장하자 과학자들은 이를 적용할 수 있는 다른 유전성 질환에도 관심을 보이기 시작했다. 지난 2월 네이처에는 신경발달장애인 스니더스 블록-캄포 증후군(Snijders Blok-Campeau syndrome)을 유전자 편집으로 개선한 연구 결과가 발표되었다. 2018년 임상 유전학자인 롯 스니더스 블록과 필립 캄포 연구팀에 의해 처음 보고된 이 질환은 대두증과 언어 발달 장애, 지적 장애를 동반한 신경발달 증후군이다. 환자 수는 전 세계적으로 수십 명 수준에 불과하여 매우 드문 질환이지만, 발생 원인은 'CHD3 유전자 돌연변이'로 매우 분명한 편이다. 세포 안에 있는 DNA는 보통 히스톤 단백질이라는 물체에 실타래처럼 꽁꽁 묶인 상태로 보관되어 있다가 필요할 때마다 풀어지며 단백질을 만들어낸다. CHD3는 히스톤 단백질에 묶여 있는 DNA를 적절한 시기에 풀었다 감아주면서 유전자가 적시에 발현되도록 돕는 유전자 중 하나이다. CHD3 유전자가 제대로 작동하지 않으면 뇌세포가 적절한 시기에 분화하고 이동하는 과정이 교란되고, 그 결과 뇌 발달에 문제가 생긴다.
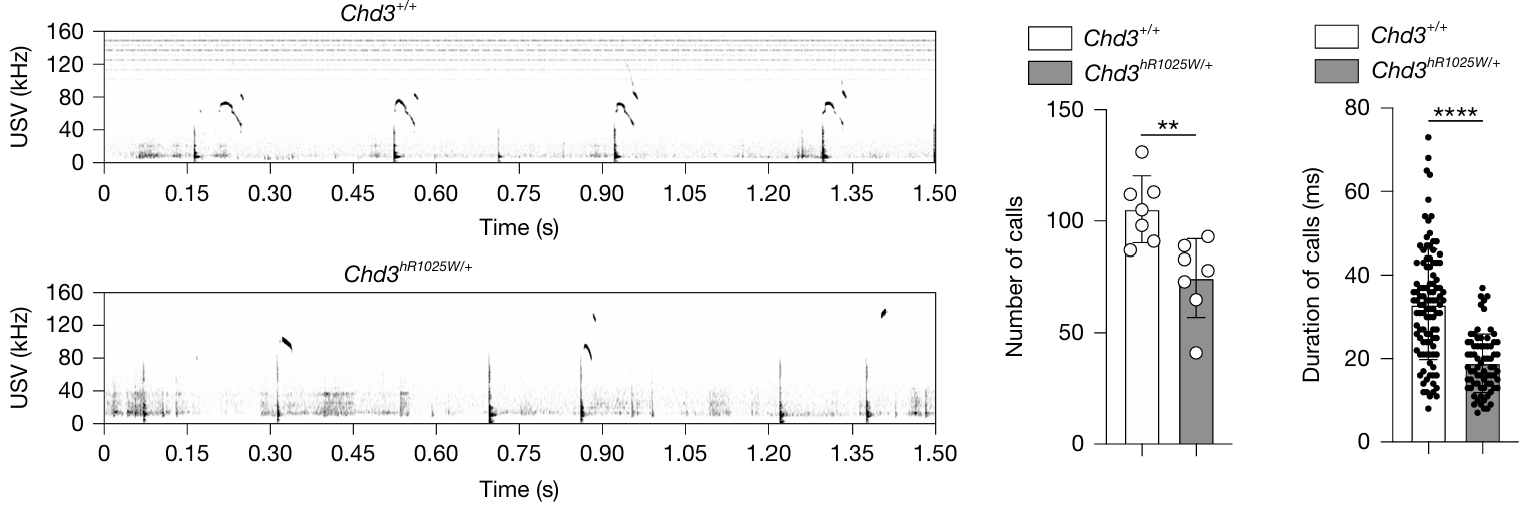
연구팀은 스니더스 블록-캠프 증후군을 겪는 환자들에게서 반복적으로 발견되는 CHD3 돌연변이 형태를 파악하여, 이를 마우스 모델에 적용하였다. 실제로 이 돌연변이를 가진 마우스는 사람 환자와 비슷한 증상을 보였다. 정상 마우스는 생후 며칠 동안 어미와 떼어 놓으면 배고픔과 외로움을 표현하는 다양한 초음파 울음소리를 냈지만, 돌연변이가 있는 마우스는 울음의 횟수와 길이가 현저히 적었다. 성체가 되고 나서도 학습 및 기억 능력과 다른 마우스와 사교하는 태도가 떨어졌는데, 이는 인간 환자에게서 관찰되는 인지 기능 장애, 사회성 저하와 유사한 결과이다.
DNA의 한 글자만 고치는 염기 편집 기술
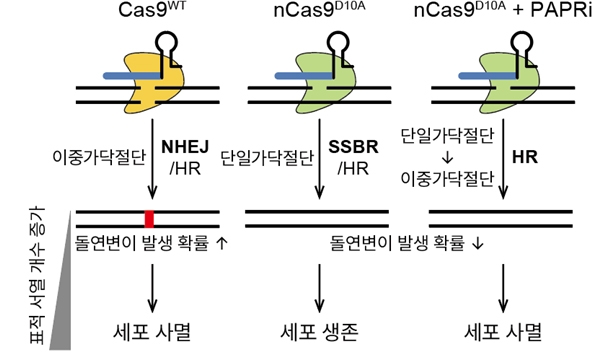
연구팀은 CHD3 돌연변이를 바로잡으면 증상이 회복될 수 있는지 확인하기 위해 염기 편집(base editing)이라는 최신 유전자 교정 기술을 사용하였다. 염기는 DNA 서열을 이루는 가장 작은 글자 단위이다. 기존 크리스퍼 유전자 가위가 잘못 적힌 문장을 고치기 위해 문장 한가운데를 크게 잘라낸 뒤 다시 이어 붙이는 방식이라면, 염기 편집은 오탈자 한 글자만 정확히 지웠다가 고쳐 쓰는 방식이다. DNA를 통째로 끊지 않고 필요한 글자 하나만 바꾸기 때문에 보다 정밀하게 DNA를 수정할 수 있고 불필요한 손상 가능성도 줄일 수 있다. 스니더스 블록-캄포 증후군을 일으키는 CHD3 돌연변이의 상당수는 단일 염기 이상으로 발생하기 때문에 염기 편집 기술의 장점을 잘 활용한 것이다.
한가지 문제점은 돌연변이가 일어난 뇌세포 안에서 염기 편집이 일어나기 위해서는 염기 편집에 사용되는 단백질과 효소들이 뇌로 전달되어야 하는데, 크기가 너무 커서 어렵다는 것이다. 이를 해결하기 위해 전체 염기 편집기를 두 부분으로 나누어 각각 다른 전달체에 싣고 동시에 뇌에 전달하여 뇌세포 내부에서 염기 편집기가 조직되도록 만들었다. 그 결과 뇌세포 안에서 정확한 염기 편집이 이루어졌고 CHD3 단백질도 정상 수준으로 회복되었다. 염기 편집이 이루어진 마우스의 다양한 행동 이상도 크게 개선되었는데, 주목할 만한 점은 치료 시점이다. 연구진은 갓 태어난 개체가 아닌 청소년기에 해당하는 시기의 마우스에 염기 편집을 적용했음에도 치료 효과가 나타났다. 이는 CHD3 단백질이 태아기뿐 아니라 출생 후에도 뇌 기능 유지에 필요하며, 돌연변이 교정이 뒤늦게라도 증상 개선에 도움이 될 수 있음을 의미한다.

SF적 상상이 치료 기술로 쓰이려면
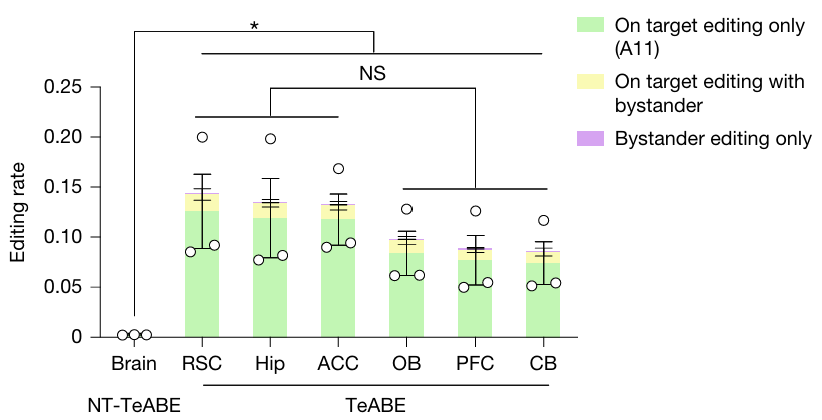
이번 연구는 단일 유전자 교정만으로 신경발달장애가 치료될 수 있다는 가능성을 보여주었다. 물론 실제 치료에 적용하려면 해결해야 할 과제도 많다. 우선 뇌에 안전하게 전달할 수 있는 운반체가 아직 확보되지 않았다. 현재는 지질 나노입자 또는 바이러스를 이용해 혈관이나 뇌에 직접 주사하는 방법이 논의되고 있다. 하지만 사람의 뇌는 혈뇌장벽이라는 강력한 방어막을 갖추고 있어 약물이 통과하기 어렵고, 장기간 안전성에 대한 검증도 필요하다. 편집 효율을 높이는 것도 필요하다. 이번 연구에서는 두 개의 전달체로 나누어 전달되었기 때문에 약 10~15%의 세포에서만 실질적인 염기 편집이 이루어졌다.
그럼에도 이번 연구는 원인이 분명한 희귀질환에서는 염기 편집 기술이 돌파구가 될 수 있음을 확인해 주었다. 앞으로 혈뇌장벽을 통과하는 전달체가 개발되고, 치료 효율로 높이는 기술이 개발된다면 스니더스 블록-캄포 증후군뿐 아니라 다른 단일 염기 돌연변이 질환에도 적용될 여지가 있다. SF 속 이야기였던 유전자 교정이 현실에서 병을 고치는 평범한 도구가 되는 날이 머지않기를 기대해 본다.
관련 연구 바로 보러 가기
In vivo base editing of Chd3 rescues behavioural abnormalities in mice, Yang et al., 2026, Nature
- 정회빈 리포터
- acochi@hanmail.net
- 저작권자 2026-03-18 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터