타우 단백질, 세포 기전에 초점
알츠하이머 치매의 주범으로 꼽히는 '타우(tau) 단백질'. 이 끈적한 단백질이 뇌에 비정상적으로 쌓이면 신경세포를 죽게 만들어 전두측두엽치매를 비롯한 여러 퇴행성 뇌질환을 일으킨다. 하지만 어떤 뇌세포는 끝까지 버티고 어떤 세포는 일찍 무너지는지, 특히 뇌에 타우가 쌓여도 인지능력을 유지하는 이른바 ‘치매 회복탄력성(Resilience)’에 대한 세포 내 기전은 오랫동안 알려지지 않았다. 타우를 직접 겨냥한 항체·백신이 치료제가 잇따라 임상에서 실패한 것도 결국 이 질문에 답하지 못했기 때문이라는 반성이 커지는 상황이었다.
이런 가운데 최근 미국 샌프란시스코 캘리포니아대(UCSF) 마틴 캠프만 교수 연구팀이 인간의 세포가 타우 단백질을 어떻게 관리하는지에 대한 근본적인 원리를 규명해 국제학술지 셀(Cell) 3월호에 발표했다.
연구진은 사람의 줄기세포에서 만든 뉴런에 유전자억제기술(이하 CRISPRi)을 동원해 타우 축적을 키우는 유전자와 줄이는 유전자를 인간 유전체 전체를 대상으로 한꺼번에 찾아내는 방식을 택했다. 이로써 뇌 속에 쌓이는 쓰레기 단백질을 제거하기 위한 분투가 세포 스스로 타우 단백질을 관리하고 파괴하는 내부 정화 시스템으로 옮겨가는 가능성을 열게 됐다.
인간 뉴런에서 찾아낸 타우 조절 유전자 1,143개
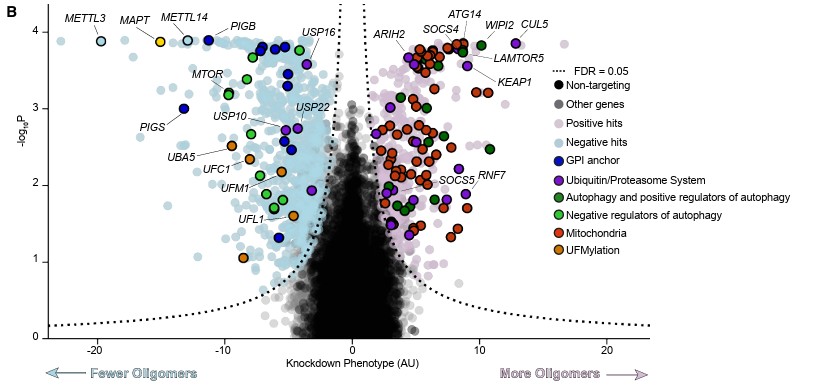
연구팀이 이번에 찾아낸 타우 조절 유전자는 무려 1,143개다. 한 번의 스크리닝으로 사람의 뉴런에서 타우 올리고머 수준에 관여하는 유전자를 이 규모로 뽑아낸 것은 처음이다.
타우 올리고머, 즉 타우가 완전히 섬유로 굳어지기 전 단계의 초기 응집체 수준을 올리거나 내리는 데 관여하는 유전자들이다. 올리고머는 완성된 섬유보다 신경세포 독성이 더 높은 것으로 알려져 있어 병리의 가장 이른 신호를 포착하기에 적합한 지표라는 게 연구진의 설명이다.
실험 모델로는 전두측두엽치매를 일으키는 유도만능줄기세포(iPSC)에서 뉴런을 만들어 실험에 사용했다. 이 변이형 타우는 알츠하이머병 환자 뇌의 타우와 섬유 구조가 같아 두 질환 모두에 적용 가능한 조절 인자를 한 모델에서 찾을 수 있다는 장점이 있다.
연구진은 타우 올리고머에 특이적으로 결합하는 항체 T22로 뉴런을 염색한 뒤, 올리고머가 많이 쌓인 세포와 적게 쌓인 세포를 형광세포분리기(FACS)로 가려냈다. 여기에 인간 단백질 암호화 유전자 전체를 하나씩 억제하는 CRISPRi 라이브러리(sgRNA 10만여 종)를 도입해 특정 유전자를 억제했을 때 타우 올리고머가 늘어나는지 줄어드는지를 차세대염기서열분석으로 읽어냈다.
확인된 1,143개 유전자에는 단백질 분해를 담당하는 자가포식·유비퀴틴-프로테아좀 시스템, 세포 에너지를 생산하는 미토콘드리아 호흡(산화적 인산화), RNA 메틸화(m6A) 관련 경로가 포함됐다. 그동안 타우 병리와 직접 연결된 적이 거의 없던 단백질 수식 경로(UFMylation)과 세포막 단백질 고정 구조(GPI anchor 생합성)도 타우 올리고머를 조절하는 새로운 축으로 확인됐다.
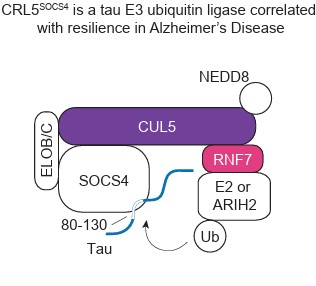
CUL5–SOCS4, 타우를 직접 분해 표지하는 단백질 복합체로 밝혀져
1,143개 유전자 가운데 연구진이 가장 깊이 파고든 것은 CUL5–SOCS4 복합체였다. 이 복합체는 세포 안에서 불필요한 단백질을 골라 ‘분해’ 꼬리표를 붙이는 역할을 하는 ‘E3 유비퀴틴 리가아제’이며, 이는 이번 연구에서 처음 밝혀졌다.
CUL5는 이 꼬리표를 붙이는 복합체의 뼈대 역할을 하고, SOCS4는 그 복합체에 붙어 표적 단백질을 골라 인식하는 어댑터 역할을 한다. 연구진은 2차 스크린과 생화학 실험을 통해 이 복합체가 타우에 직접 유비퀴틴을 붙인다는 것을 확인했다. CUL5–SOCS4가 제대로 작동하면 타우는 분해 경로로 보내지고, 기능이 떨어지면 타우가 뉴런 안에 그대로 쌓인다.
나아가 연구팀은 알츠하이머병·전두측두엽치매·진행성 핵상 마비(PSP) 환자의 뇌 조직 단세포 전사체 자료를 분석했다. 그 결과 CUL5 복합체 관련 유전자 발현이 높은 뉴런일수록 질환이 진행된 뇌에서도 더 오래 생존하는 경향이 확인됐다. 앞서 제기한 '치매 회복탄력성'의 분자적 근거 중 하나가 바로 이 시스템에 있을 수 있다는 것이다. 교신저자 캄프만 교수는 "이 경로의 발현이 실제 환자 뇌에서 뉴런 생존과 연결된다는 사실은 타우병 치료 전략의 새로운 표적이 될 수 있음을 시사한다"고 말했다.
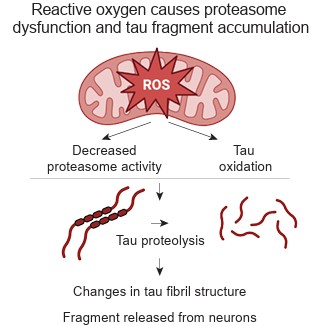
미토콘드리아가 망가지면 독성 타우 조각이 만들어져 분비돼
이번 연구가 밝혀낸 또 하나의 중요한 발견은 미토콘드리아 손상과 타우 병리의 연결고리다. 스크린 결과에서 미토콘드리아 호흡(산화적 인산화) 관련 유전자를 억제했을 때 타우 올리고머가 가장 강하게 증가했다. 연구진은 그 안에서 일어나는 일을 단계별로 추적했다.
미토콘드리아는 세포가 살아가는 데 필요한 에너지를 만드는 기관이다. 이 기능이 떨어지면 세포 안에 활성산소(ROS)가 쌓이고, 활성산소는 단백질 분해 기계인 프로테아좀을 손상시킨다. 결국 이 시스템은 세포 안에서 낡거나 불필요한 단백질을 잘게 잘라 처리하는 역할을 하는데, 이 기계가 망가지자 타우가 비정상적으로 잘려 약 25kDa 크기의 특정 타우 조각이 뉴런 안에 쌓이기 시작했다.
문제는 이 조각이 세포 안에 머무르지 않는다는 점이다. 뉴런 밖으로 분비됐고, 알츠하이머병 바이오마커로 주목받는 ‘N-말단 아세틸화(NTA) 타우 항체’에 양성 반응을 보였다. 시험관 실험에서는 이 조각이 정상 타우 단백질과 함께 있을 때 타우 섬유화 속도와 최종 구조까지 바꿔놓는 것이 확인됐다.
연구진은 "활성산소에 의해 손상된 프로테아좀이 만들어낸 이 조각이 알츠하이머병 관련 바이오마커 형태로 분비되고, 타우 응집의 구조와 속도까지 바꾼다는 점에서 질환 관련성이 높다"고 설명했다. 뇌에 타우가 얼마나 쌓였는지만큼 미토콘드리아 기능 저하가 어떤 타우 조각을 만들어내는지도 질환의 경과를 좌우할 수 있다는 것이다.
타우 치료, 단백질 하나에서 세포 시스템 전체로
이번 연구는 인간 뉴런 수준에서 타우 항상성을 조절하는 경로의 전체 지도를 처음으로 그렸다는 데 의미가 있다. 하지만 세포 수준의 결과를 치료제로 이어가려면 동물 모델 검증과 임상 안전성 확인이라는 긴 과정이 남아 있다.
캄프만 교수는 "이번 연구는 인간 뉴런에서 타우 단백질 항상성의 원리를 체계적으로 밝히고, 타우병 치료를 위한 잠재적 표적들을 제시한다"고 밝혔다. 이어 그는 타우병 치료의 다음 단계는 타우 단백질 하나를 겨냥하는 것에서, 세포 스스로 타우를 관리하는 내부 시스템 전체를 이해하고 그 안에서 표적을 찾는 방향으로 가야 한다고 말했다.
- 김현정 리포터
- vegastar0707@gmail.com
- 저작권자 2026-03-19 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터