올해 북미에서 사람이 H5N1형 고병원성 조류인플루엔자(AI) 감염으로 사망한 사례가 잇따르는 가운데 국내 연구진이 북미형 H5N1 바이러스가 포유류에서 치명적인 이유를 밝혔다.
기초과학연구원(IBS)은 한국바이러스기초연구소 최영기 소장 연구팀이 북미형 H5N1 AI 바이러스가 포유류에서 치명적인 병원성을 일으키는 원인을 규명했다고 29일 밝혔다.
2022년 처음 보고된 북미형 H5N1 AI는 전신 확산과 높은 치명률을 특징으로 하는 새로운 유전자 조합의 고병원성 AI다.
단순한 호흡기 감염을 넘어 면역세포까지 감염시키며, 전신으로 퍼져 뇌까지 침투하는 특징을 보인다.
지난해 3월 이후 미국 10여 개 주의 낙농 농가에서 젖소 집단 감염이 확인됐다.
감염된 젖소의 젖에서 바이러스 유전 물질이 검출되며 모유 전파 가능성까지 제기됐고, 고양이 등 다른 포유류뿐 아니라 사람까지 감염시키는 사례가 잇따라 보고되며 국제 사회의 우려가 커지고 있다.
하지만 북미형 H5N1 바이러스가 포유류에 치명적인 이유는 알려지지 않았다.
연구팀은 특정 변이가 전신 확산과 신경계 침투를 매개하는 핵심 요인임을 확인했다.
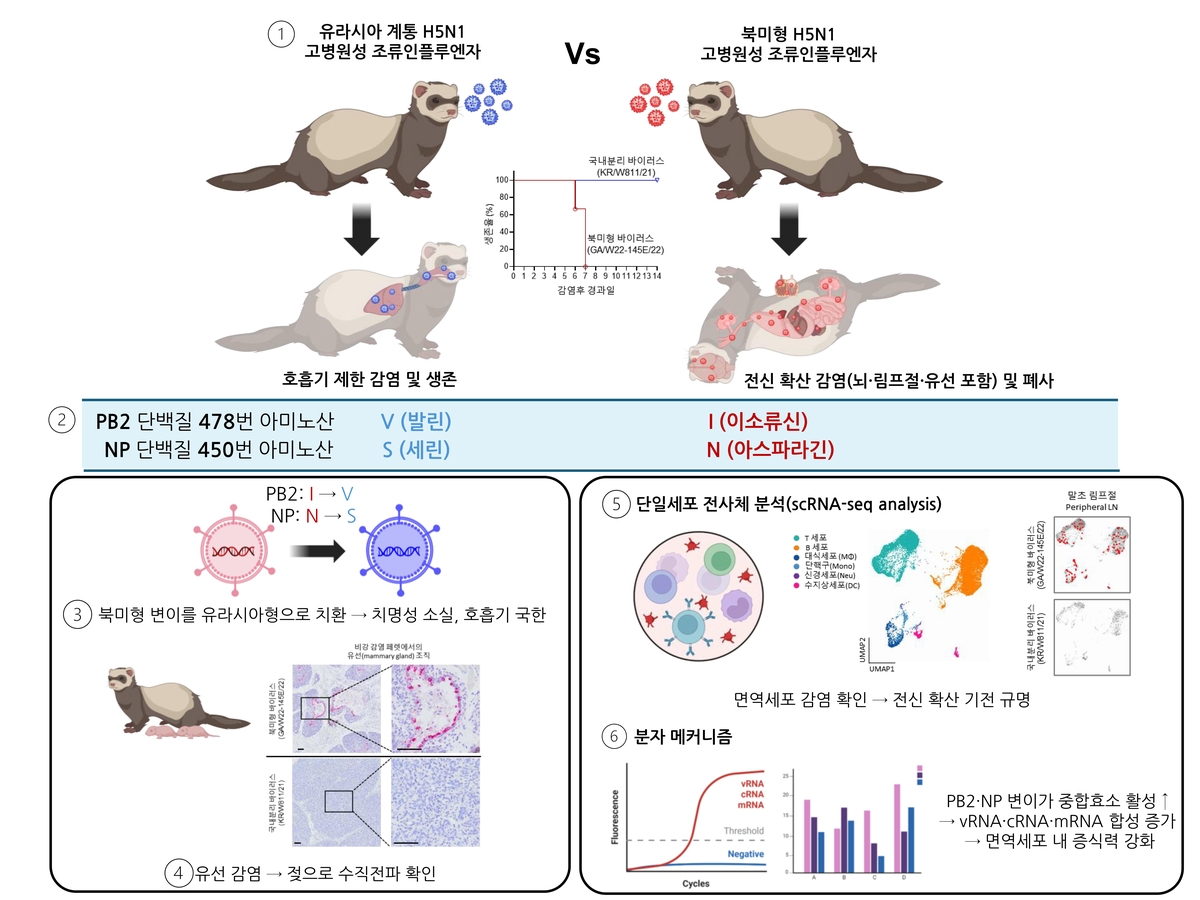
북미형 H5N1 바이러스 'GA/W22-145E/22'와 한국에서 확보한 유라시아 계통의 동일 아형 H5N1 바이러스 'KR/W811/21'을 비교해 병원성 차이를 분석했다.
북미형은 족제빗과 포유류인 페럿 감염 모델 실험에서 일주일 이내 100% 치사율을 보였다.
뇌와 림프절을 포함한 전신 감염을 일으켰고, 젖을 분비하는 유선까지 감염이 확산해 모유 매개 전파 가능성도 확인됐다.
반면 유라시아형은 호흡기 감염에 국한되며 병원성이 낮은 것으로 나타났다.
연구팀은 북미형 바이러스가 T세포, B세포, 대식세포 등 다양한 면역세포에서 검출됨을 확인했다.
연구팀이 북미형에서 발견된 두 아미노산 변이를 유라시아형 아미노산으로 바꿔 제작한 바이러스를 감염 실험한 결과, 병원성이 크게 약화하고 감염이 호흡기로 제한된 것으로 나타났다.
두 개의 변이는 바이러스의 유전체 복제 효율을 높여 포유류 세포 내에서 복제력을 강화함을 확인했다.
이는 두 변이가 H5N1 바이러스의 포유류 적응성과 병원성 강화를 이끄는 핵심 요인임을 보여준다.
이와 함께 소에서 유래한 유선 오가노이드(인공 장기)에 북미형 H5N1을 감염시켜 증식양상을 분석한 결과, 북미형은 유선 오가노이드 조직에서 활발히 증식했으나 유라시아형이나 변이를 유라시아형으로 바꾼 바이러스의 증식은 제한적인 것으로 나타났다.
연구팀은 출산한 페럿 감염 모델을 이용해 모유 전파 가능성도 확인했다.
감염된 어미의 뇌에서도 바이러스가 검출돼 전신 확산이 확인됐으며, 유선에서 증식한 바이러스가 실제로 모유를 통해 새끼로 전파되는 양상이 관찰됐다.
최영기 소장은 "유럽과 아시아의 철새들이 북미로 이동해 H5N1 바이러스의 변이를 일으켜 치명성을 높인 것이 북미형 H5N1으로, 다시 유라시아로 날아올 가능성도 있다"며 "고병원성 조류인플루엔자가 새로운 팬데믹의 잠재적 위협이 되는 만큼, 인체와 가축 간 교차 감염병 확산 위험에 선제적으로 대응할 필요가 있다"고 말했다.
이번 연구 결과는 권위 있는 과학 학술지 '사이언스 어드밴시스'(Science Advances) 지난 27일 자에 실렸다.
- 연합뉴스
- 저작권자 2025-09-30 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터



















