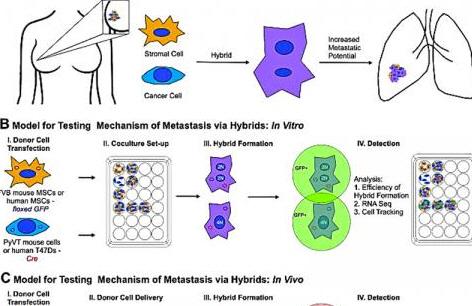
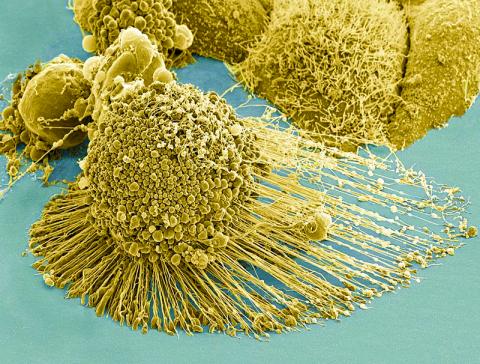
암세포는 유전적 혼란을 일으키는 것으로 알려져 있다. 암세포가 분열함에 따라 DNA 세그먼트를 비롯해 심지어는 염색체 전체가 복제되거나 변이 혹은 완전히 소실될 수 있기 때문이다. 이를 염색체 불안전성(chromosomal instability)이라 부른다.
최근 미국 슬로언 케터링 암센터(MSK) 연구팀은 이 같은 염색체 불안정성이 암의 공격성과 관련돼 있다는 사실을 밝혀내 종양 전문저널 ‘암 디스커버리’(Cancer Discovery) 28일 자에 보고했다.
이번 연구는 암세포가 면역을 회피하는 방법을 구체적으로 밝혀내는 것 외에, 차단 약물을 개발함으로써 현재 몇몇 유형의 암들에 대해 효과가 미미한 면역항암요법의 민감도를 한층 높일 수 있을 것으로 기대되고 있다.
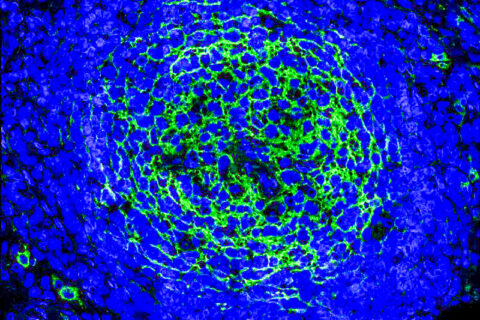
암세포는 어떻게 면역반응을 회피하나
염색체가 불안정할수록 염색체의 DNA 조각들은 원래 있던 곳에서 벗어날 가능성이 더 높아진다. 즉 세포의 중심핵 바깥으로 벗어나 있거나 세포질 안을 떠다니는 것이다.
세포는 이런 불량 DNA 조각을 바이러스 침입의 증거로 해석해 내부 경보를 울리고 염증을 유발한다. 이렇게 되면 면역세포들이 종양 부위로 이동해 방어 화학물질을 대량으로 방출한다.
문제는 암세포에 의해 촉발된 이 같은 면역반응이 실제로는 암세포를 몰락시키지 않는다는 점이다.
MSK 의사이자 과학자로 ‘인간 종양 및 발병 프로그램’ 멤버인 새뮤얼 배쿰(Samuel Bakhoum) 박사는 “우리가 알면서도 제대로 말을 못했던 것은 암세포들이 어떻게 (면역세포로 인한) 염증성 환경에서 생존하고 번성할 수 있는지를 이해하지 못했다는 점”이라고 지적했다.
배쿰 박사팀은 이번 연구에서 그 이유가 부분적으로는 암세포 바깥에 위치한 분자와 관련이 있다고 밝혔다. 즉 경고 신호가 이웃 면역세포들에 도달하기 전에 분자 하나가 이 신호들을 파괴한다는 것이다.
이 연구 결과는 일부 종양이 면역요법에 반응하지 않는 이유 설명에 도움이 되는 한편, 이 종양들이 면역요법에 반응하도록 하는 방법들을 제시해 주목된다.
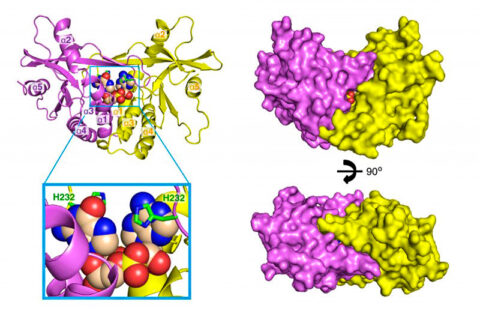
위험한 DNA를 탐지
배쿰 박사팀은 cGAS-STING라고 불리는 경고 시스템을 연구해 왔다. 바이러스 혹은 불안정한 암 염색체의 DNA가 세포질로 떨어져 나오면 cGAS 아미노산 단백질이 그와 결합해 경고 신호 역할을 하는 cGAMP라는 화합물 분자를 만든다.
세포 내부에서 이 경고 신호가 발령되면 잠재적인 바이러스 침입이라는 즉각적인 문제 해결을 위해 STING이라는 면역반응을 활성화시킨다.
또한 cGAMP 분자의 대부분은 세포 외부로 이동해 인접한 면역세포들에게 경고 신호 역할을 한다. 이는 STING 면역반응 경로를 활성화해 바이러스에 감염된 세포에 대한 면역 공격을 불러일으키게 된다.
배쿰 박사팀은 이전 연구에서 암세포 내부에서의 cGAS-STING 신호가 암세포들로 하여금 면역세포의 특성, 특히 기어서 이동하는 능력을 채택하도록 함으로써 전이 능력을 돕는다는 사실을 밝혀낸 바 있다.
이 연구를 통해 암세포가 어떻게 염증 환경에서 살아남고 그 과정에서 전이를 돕는지에 대한 일부 해답이 제시됐다.
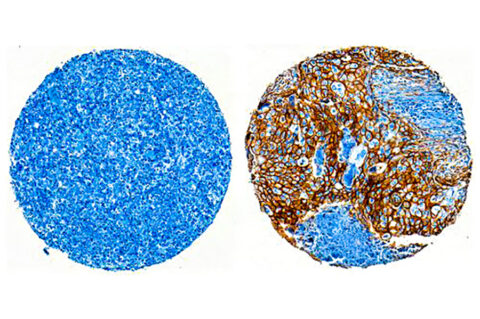
ENPP1, 면역 억제와 암 전이 조절 스위치
이번 새로운 연구에서는 암세포들이 환경으로 방출된 활성화된 cGAS-STING의 경고 신호에 어떻게 대처하는지를 보여주었다. 즉, 가위 모양으로 생긴 단백질이 신호를 파쇄해 면역 공격의 위협을 막을 수 있는 두 번째 방법을 제시했다.
암세포를 덮고 있는 가위 모양의 단백질은 ENPP1이라고 불린다. cGAMP가 세포 밖에서 길을 찾을 때 ENPP1이 이를 잘라내 신호가 면역세포에 도달하는 것을 차단하는 동시에, 이 절단을 통해 아데노신이라는 면역 억제 분자를 방출해 염증을 진정시킨다는 것.
배쿰 박사팀은 유방암과 폐암, 대장암 쥐 모델을 이용한 일련의 실험을 통해 ENPP1이 면역 억제와 전이의 조절 스위치 역할을 한다는 사실을 보여주었다.
이 스위치를 켜면 면역 반응이 억제되고 전이가 증가하며, 반대로 스위치를 끄면 면역 반응이 활성화되고 전이가 줄어들었다.
연구팀이 사람의 암 표본에서 ENPP1을 살펴본 결과, 이 단백질 발현이 전이 증가 및 면역요법에 대한 내성과 상관관계가 있는 것으로 나타났다.

면역요법 강화를 위해
치료의 관점에서 볼 때 이번 연구에서 가장 주목할 만한 사실은 ENPP1 스위치를 끄면 관문 억제제로 불리는 면역치료제에 대한 여러 암들의 약물 반응 민감도를 높일 수 있다는 점이다. 연구팀은 이 접근법이 쥐의 암 모델에서 효과적이라는 사실을 보여주었다.
현재 암세포에서 ENPP1을 억제하는 약물이 배쿰 박사팀이 설립한 회사를 포함한 여러 회사들에서 개발되고 있다. 배쿰 박사는 ENPP1이 다행스럽게도 암세포 표면에 있어 차단 약물이 이를 쉽게 표적화할 수 있다고 말했다.
해당 약물은 또한 상대적인 목표 특이성을 지니고 있는 것으로 알려졌다. 건강한 개인의 조직에는 대부분 염증이 없기 때문에 ENPP1을 표적으로 하는 약물은 주로 암에만 영향을 미친다는 것.
ENPP1을 표적화하면 두 가지 다른 방법으로 암을 약화시킨다. 배쿰 박사는 “암세포 외부에서 cGAMP 분자 수준을 동시에 증가시켜 인접 면역세포에서의 STING 면역반응을 활성화하면서 면역 억제 아데노신 생성을 차단할 수 있다”며, “일석이조의 효과를 얻는 셈”이라고 설명했다.
배쿰 박사는 이번 연구 속도가 매우 빨랐다고 말했다. 2018년에 시작한 연구가 이제 곧 환자들에게 도움이 될 것으로 보여 매우 자랑스럽다는 것. 그는 1년 이내에 ENPP1 억제제 임상 1상 시험이 이뤄질 것으로 기대하고 있다.
- 김병희 객원기자
- hanbit7@gmail.com
- 저작권자 2021-01-04 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터