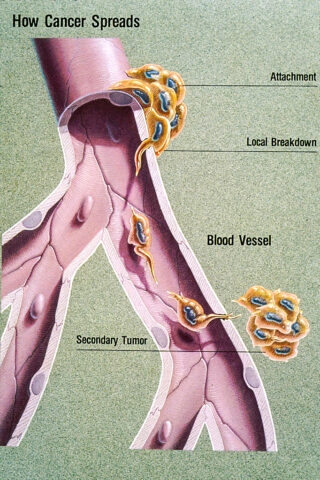
주위에서 암이 전이돼 고생하는 환자들을 더러 볼 수 있다. 암이 전이되는 것은 암세포가 혈관으로 이동해 혈류를 타고 인체 다른 부위로 옮겨가 종양을 유발하기 때문이다.
이런 암세포를 비롯해 인체의 면역세포 등 각종 세포들은 어떻게 움직이는 것일까?
세포가 움직이는 것은 경로 표면의 끈적임에 따라 달라지는 것으로 알려져 있다. 그러나 이 정확한 메커니즘은 지난 수십 년 동안 제대로 알려지지 않았었다.
최근 독일헬름홀츠협회 막스 델브뤼크 분자의학센터(MDC)와 뮌헨 루드비히 막시밀리안대(LMU) 연구팀이 세포 이동의 정확한 역학을 파악하고, 세포 이동과 관련된 힘을 포착할 수 있는 수학 모델을 개발해 미국 국립과학원 회보(PNAS) 최근호에 발표했다.
연구팀은 이번 발견이 발달생물학과 암 치료에 새로운 통찰을 제시할 것으로 보고 있다.
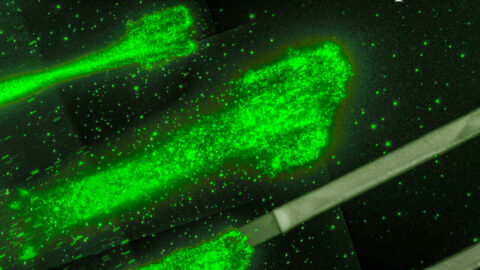
세포 이동은 세포 활동의 기본 과정으로, 특히 초기 세포가 어떤 표적 세포 유형으로 분화한 다음 그에 해당하는 조직으로 이동할 때의 발달단계에서 중요한 역할을 한다.
세포들은 또한 상처를 복구하기 위해 이동하는 반면, 암세포는 가장 가까운 혈관으로 기어가 혈관을 타고 다른 인체 부위로 퍼져나간다.
MDC 수리 세포생물학 연구실을 이끌며 이번 연구를 공동으로 주도한 마르틴 팔케(Martin Falcke) 교수는 “이번에 개발한 수리 모델은 연구자들이 다양한 세포가 다양한 기질에서 어떻게 행동할지를 예측하는데 활용할 수 있다”며, “이런 기본적인 움직임을 정밀하게 이해하면 암 전이를 차단하는 새로운 표적을 제시할 수 있을 것”이라고 밝혔다.
실험과 이론 연구팀 연합해 성과 올려
저자들은 이번 발견이 LMU의 실험 물리학자들과 MDC의 이론 물리학자들이 서로 협력해 일궈낸 성과라고 말했다.
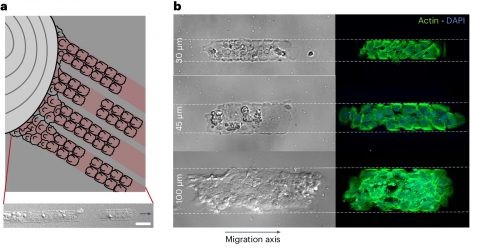
LMU의 요아킴 래들러(Joachim Rädler) 교수가 이끄는 실험팀은 1만 5000개 이상의 암세포들이 표면이 끈적끈적한 좁은 경로를 따라 얼마나 빠르게 이동했는지를 추적했다. 끈적임의 정도는 위치에 따라 심하거나 덜했다.
래들러 교수팀은 이를 통해 세포가 이동할 때 끈적임 정도에 따라 어떤 일이 일어나는지를 관찰해, 신체 내부의 역동적 환경을 더욱 잘 파악할 수 있었다.
이어 MDC의 팔케 교수와, 논문 공동 제1저자인 베남 아미리(Behnam Amiri) 박사과정 연구원은 대규모 데이터세트를 사용해, 세포의 운동성 형성 요소들을 포착할 수 있는 수학 방정식을 개발했다.
아미리 연구원은 “세포 이동과 운동성을 설명하려는 이전의 수학 모델은 매우 제한적이어서 세포의 한 가지 특성이나 한 세포 유형에서만 작동한다”고 지적하고, “이번 연구에서 우리는 가능한 한 간단하고 일반성을 가진 모델을 만들 수 있도록 노력했다”고 말했다.
이 접근 방식은 예상보다 훨씬 더 잘 작동했다. 개발된 모델은 LMU에서 수집한 데이터와 일치했고, 지난 30년 동안 축적된 여러 다른 세포 유형에 대한 측정 결과도 정확했다.
팔케 교수는 “결과가 놀랍다”며, “그렇게 광범위한 실험 결과를 설명할 수 있는 이론을 찾기는 힘들다”고 전했다.
마찰이 열쇠
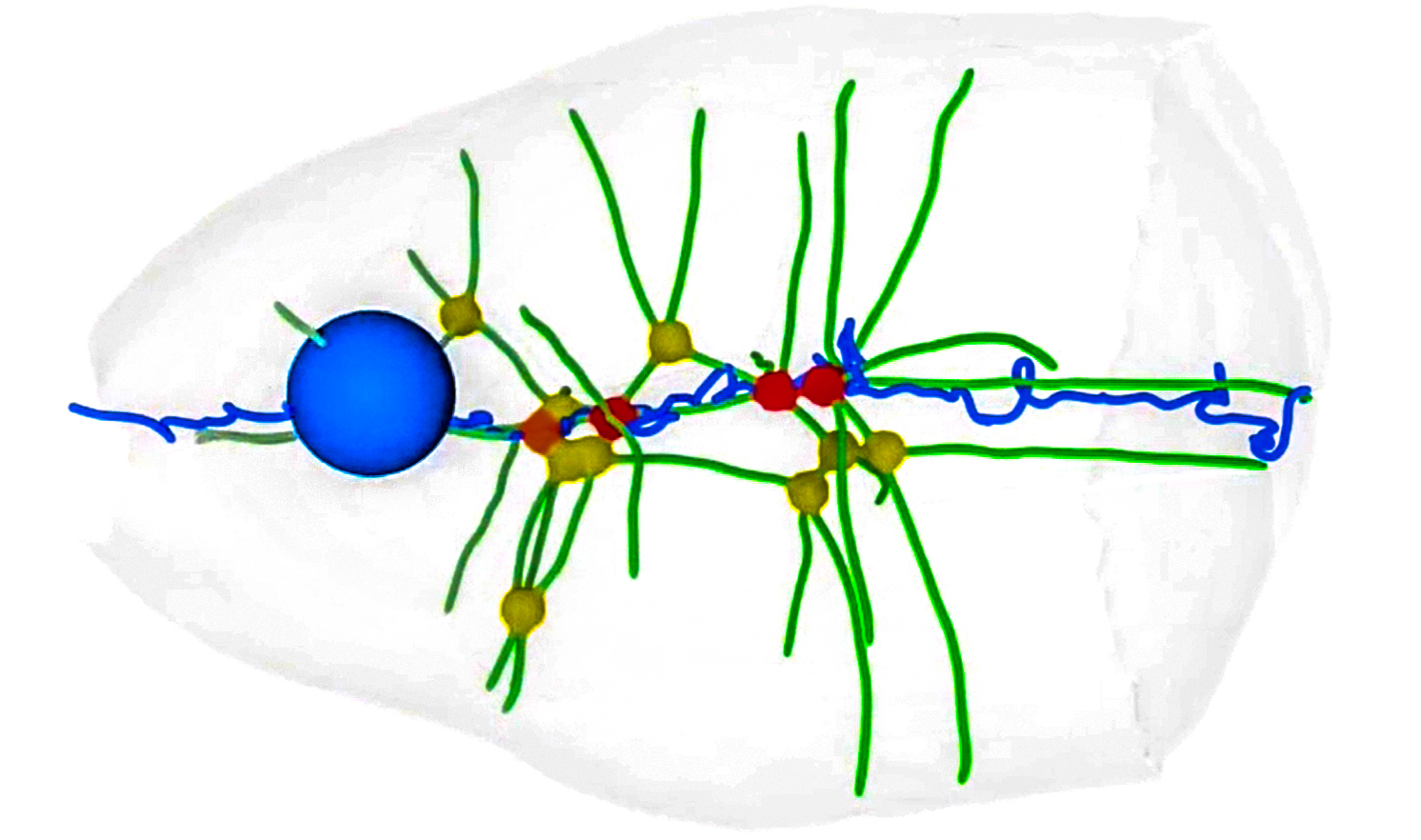
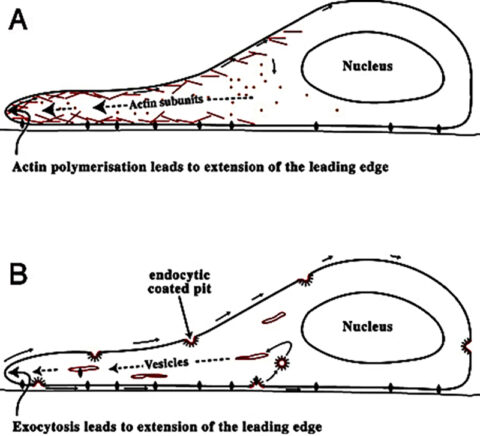
세포가 움직일 때는 이동 방향으로 세포막을 밀어내 근육 수축에 필요한 단백질의 일종인 액틴 필라멘트의 내부 네트워크를 확장시킨 다음 뒤쪽 끝을 표면에서 떼어낸다.
이 일이 얼마나 빨리 일어나는가는 세포와 이 세포 아래의 표면 사이에 형성되는 접합 결합에 달려있다. 결합이 존재하지 않으면 액틴 네크워크가 밀어낼 것이 없기 때문에 거의 움직일 수가 없다.
그 이유는 바로 마찰에 있다. 팔케 교수는 “얼음 위에서 썰매를 타고 앞에 있는 차를 밀어낼 수 없듯이, 신발과 지면 사이에 충분한 마찰이 있을 때만 차를 밀 수 있다”고 말했다.
결합 수가 증가해 마찰이 증대됨에 따라 세포는 더 많은 힘을 생성해 더 빠르게 움직일 수 있다. 그러나 너무 끈적거리는 지점에 이르면 세포 뒤쪽 끝을 끌어당기기가 어려워져서 속도는 다시 느려지게 된다.
느려지지만 달라붙지는 않아
연구팀은 세포 앞뒤 끝의 끈적임 정도가 서로 다를 때 어떤 일이 일어나는지를 조사했다. 이들은 특히 세포 뒤쪽 끝의 아래 표면이 앞쪽보다 더 끈적거릴 때의 상황을 궁금해했는데, 그 이유는 세포가 뒤쪽 끝을 끌어당길 충분한 힘이 없으면 표면에 달라붙어 고착될 가능성이 있을 것으로 생각했기 때문이다.
만약 접착 결합이 나사와 비슷하게 세포를 접촉 표면의 기질에 고정시킨다면 그럴 가능성이 있다. 처음에 팔케 교수와 아미리 연구원은 이런 종류의 ‘탄성(elastic)’ 힘을 모델에 포함시켰으나 방정식은 마찰력으로만 작동했다.
팔케 교수는 “가장 어려웠던 부분은 이 메커니즘이 오직 마찰력으로만 작동한다는 점”이었다며, 그럴 경우 세포가 단단히 붙어있을 곳이 아무 데도 없기 때문이었다고 말했다.
그러나 마찰력 같은 힘은 뒤쪽의 접합이 앞쪽보다 더 강할 때도 스카치테이프처럼 천천히 뒤쪽 끝을 떼어내면서 세포를 계속 움직이게 했다.
팔케 교수는 “아주 약한 힘을 가해도 테이프를 천천히 떼어낼 수 있다”며, “이것이 세포가 기질에 달라붙는 것을 방지하는 방법”이라고 말했다.
연구팀은 현재 세포가 오른쪽이나 왼쪽 혹은 유턴을 포함해 2차원 공간에서 어떻게 움직이는지를 조사하고 있다.
- 김병희 객원기자
- hanbit7@gmail.com
- 저작권자 2021-01-21 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터