글 : KAIST 생명과학과 한용만 교수 연구실 최지은 박사
한국인의 삶을 고달프게 하는 국민질환 1위가 당뇨병이라는 최근 발표가 있습니다. 당뇨병은 오랜 기간 합병증을 겪으면서 환자들의 삶을 힘들게 하기 때문입니다. 당뇨병은 소변으로 포도당이 배출된다고 하여 붙여진 이름입니다. 여기에는 췌장에서 분비되는 인슐린이라는 호르몬이 중요한 작용을 합니다. 인슐린이 부족하거나 제 기능을 하지 못하면 세포에서 포도당을 에너지원으로 이용하지 못하고 혈당이 비정상적으로 올라가게 됩니다.
당뇨병은 1형과 2형으로 구분됩니다. 1형은 인슐린 분비를 담당하는 췌장 내 베타세포의 기능 저하로 인해 인슐린의 분비가 감소해서 발생되는 선천적인 질환입니다. 2형은 인슐린을 수용하는 세포에 내성이 생겨 호르몬이 제대로 기능하지 못하여 혈당이 조절되지 못하는 후천적 질환입니다. 미래에는 인슐린 분비를 자유자재로 조절할 수 있을까요?
빛으로 신경세포들의 활동을 조절하다
광유전학(optogenetics)은 말 그대로 광(opto)+유전학(genetics)의 합성어로서 유전학적 기법에 광학적 기술을 접목한 것입니다. 이 광유전학의 개념은 청색 빛을 감지하여 녹조류의 신경에 전류를 일으키고 있는 특수한 단백질, ‘채널로돕신 (Channelrhodopsin)’의 발견으로부터 시작되었습니다(2). 즉 자극을 원하는 세포에 빛을 감지하는 채널로돕신이라는 센서를 부착한 것입니다.
채널로돕신은 빛을 인지하는 센서로 작용하며 자극을 원하는 세포만을 자극 시킬 수 있도록 해줍니다. 광유전학이 나오기 전까지는 신경세포를 촉진·억제하기 위해서는 전기나 약물을 사용했습니다. 그러나 이 방법들은 주변의 다른 세포까지 영향을 줘 정교하게 신호를 조절하는 데는 어려움이 있었습니다. 무엇보다도 광유전학의 장점은 타겟 세포 혹은 타겟 세포 내의 원하는 위치만을 원하는 시각에 ON/OFF 시키는 정확성, 다시 말해 시공간적(spatiotemporal) 조절이 가능하다는 것입니다.
그동안 광유전학 기술은 신경세포 및 일반 세포를 대상으로 세포 내 분자적 메커니즘의 조절 연구에 활발히 응용되어 오고 있습니다. 여기에서는 혈당을 조절하는 주요 호르몬인 ‘인슐린’의 분비를 광유전학적으로 조절하는 내용을 소개하고자 합니다.
당뇨병 치료의 신기원 열리나?
췌장 내 베타세포의 기능 저하가 원인인 1형 당뇨의 경우 선천적으로 췌장에서 인슐린을 만들어 내지 못하기 때문에 식단 조절이나 운동 등을 통해 조절이 되지 않습니다. 정확히 정해진 시간에 인슐린을 주사하는 방법 외에는 실질적으로 치료를 할 방법이 여전히 없는 실정입니다. 따라서 당뇨병을 연구하는 과학자들은 오래전부터 췌장 베타세포의 재생 및 대체 치료에 많은 관심을 가졌습니다.
광유전학 기술을 통한 당뇨 치료기술의 아이디어적 핵심은 빛 자극을 받았을 경우에만 인슐린을 분비할 수 있는 베타세포를 제작하여 이를 환자에 이식하고자 하는 것입니다. 이를 통해 환자의 편의성을 대폭 개선함과 동시에 처방 용량의 개인별 맞춤화를 이룰 수 있게 됩니다. 이러한 아이디어는 2011년 스위스 연구팀에 의해 최초로 소개되었습니다. 멜라놉신(melanopsin) 이라는 광센서 단백질(빛을 감지하면 세포 내로 칼슘 이온을 들여보내는 성질을 가진 단백질)을 활용하여 빛을 받으면 간접적으로 인슐린을 생산하는 디자인 세포를 만드는 데에 성공하였습니다(3)(그림2).

이후 채널로돕신을 포함 여러 광센서 단백질들을 활용한 당뇨병 치료 기술이 개발되어 왔습니다(4-6). 한편, KAIST 생명과학과 허원도 교수팀은 OptoSTIM1이라는 광센서 단백질을 통한 칼슘이온 조절을 보고한 바 있습니다(7).
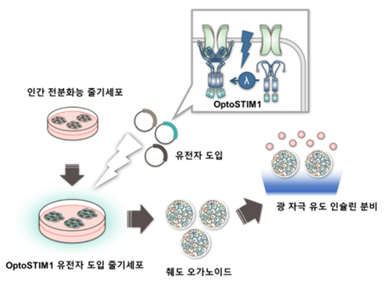
본 연구팀은 이 OptoSTIM1 광센서를 인간전분화능 줄기세포에 도입하고 이를 췌도 오가노이드(pancreatic islet-like organoid)로 분화시키는데 성공하였습니다(그림 3). 아울러 이들 췌도 오가노이드는 광 조사에 의해 인슐린을 분비할 수 있음을 확인하였습니다.
결론적으로 췌장 베타세포가 인슐린을 분비하기 위해서는 필수적으로 세포 내 칼슘 이온 농도의 증가가 선행되어야 하는데, OptoSTIM1을 베타세포에 도입함으로써 광유전학적으로 칼슘이온 증가를 통한 인슐린 분비를 유도한다는 원리입니다. 이러한 광유전학 기술이 실용화 단계에 이르기까지는 아직 넘어야 할 산이 많습니다.
그러나 빛 자극만으로 당뇨를 치료할 수 있을지도 모른다는 상상이 실질적으로도 증명되고 있다는 사실은 자못 흥미로운 일이 아닐 수 없습니다. 미래에는 정말 빛 조절 버튼 하나만으로 내 몸의 혈당을 자유자재로 조절할 수 있는 시대가 올지도 모릅니다.
[참고문헌]
1. Courtesy of the MIT McGovern Institute, Julie Pryor, Charles Jennings, Sputnik Animation , and Ed Boyden.
2. Nagel, G. et al. (2003). Channelrhodopsin-2, a directly light-gated cation-selective membrane channel. Proc Natl Acad Sci 100, 13940.
3. Ye, H. et al. (2011). A synthetic optogenetic transcription device enhances blood-glucose homeostasis in mice. Science 332, 1565.
4. Kushibiki, T. et al. (2015). Optogenetic control of insulin secretion by pancreatic beta-cells in vitro and in vivo. Gene Ther 22, 553.
5. Zhang, F., and Tzanakakis, E.S. (2019). Amelioration of Diabetes in a Murine Model upon Transplantation of Pancreatic beta-Cells with Optogenetic Control of Cyclic Adenosine Monophosphate. ACS Synth Biol 8, 2248.
6. Shao, J. et al. (2017). Smartphone-controlled optogenetically engineered cells enable semiautomatic glucose homeostasis in diabetic mice. Sci Transl Med 9. eaal2298.
7. Kyung, T. et al. (2015). Optogenetic control of endogenous Ca(2+) channels in vivo. Nat Biotechnol 33, 1092.
* 이 글은 범부처재생의료기술개발사업단(KAIST 생명과학과 한용만 교수 연구실 최지은 박사)으로부터 제공받았습니다.
- 범부처재생의료기술개발사업단
- 저작권자 2022-08-16 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터