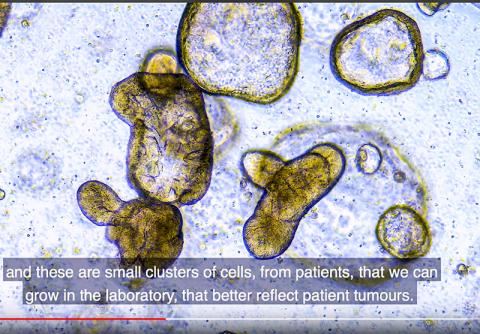
새로운 표적 암 치료제 개발에 청신호가 켜지면서 암 치료 정밀의학이 속도를 내고 있다.
크리스퍼(CRISPR) 유전자 가위 기술을 이용한 최근의 대규모 연구에서 영국의 웰컴 생어 연구소(Wellcome Sanger Institute)와, 신약 개발을 위한 세계 7개 기관 협력체인 오픈 타깃(Open Targets) 연구팀은 30개의 암 유형에서 뽑은 300개 암 모델의 모든 유전자를 정지시켜, 암이 생존하는데 필수적인 수천 개의 핵심 유전자를 발견해 내는 성과를 거뒀다.
이와 함께 치료제 개발 가능성이 가장 높은 600개 약물 표적의 우선순위를 정하고 순위를 매길 수 있는 새로운 시스템을 개발했다.
과학저널 ‘네이처’(Nature) 10일 자에 발표된 이번 연구 결과에 따라 표적 암 치료법 개발을 가속화하는 한편, 암 의존성 관계 지도(Cancer Dependency Map) 생성에도 한발 다가서게 됐다. 관련 동영상
‘암 의존성 관계 지도’는 암의 유전적 특성과 발병 경향을 밝혀 환자들이 효과적인 치료를 받을 수 있도록 돕는 정밀 암 치료법의 세부 규정집이라고 할 수 있다.
새로운 암 표적치료제의 필요성
영국에서는 2분마다 한 명씩 암 진단을 받고, 두 명 중 한 명은 생애의 어느 시점에서 암이 발병하는 것으로 추정된다.
암을 치료하기 위해 일반적으로 수술과 화학요법 및 방사선요법이 사용되지만 일부 환자는 치료 효과가 없고, 간혹 건강한 조직이 손상돼 환자에게 원치 않는 부작용을 유발하기도 한다.
이 때문에 과학자들과 제약회사는 건강한 조직에는 해를 주지 않으면서 암세포만을 선택적으로 죽이는 새로운 표적 치료법 개발에 몰두하고 있다.
효과적인 새 치료법 개발은 말처럼 그리 쉽지가 않다. 단일 치료제 하나를 개발하는데 10~20억 달러가 소요되고, 그렇게 돈을 들여도 전체의 90%는 개발 중에 실패로 돌아간다.
따라서 개발 초기에 먼저 정확한 약물 표적을 선택하는 것이 신약개발에서 가장 중요한 일로 여겨진다.

300개 암 모델에서 타깃 유전자 600개 확인
웰컴 생어 연구소와 제약회사 GSK, 유럽분자생물학연구소-유럽생물학정보연구소(EMBL-EBI), 오픈 타깃을 비롯한 공동연구팀은 현재까지 알려진 암 유전자에 대해 최대 규모의 크리스퍼(CRISPR) 검색을 수행했다.
이에 따라 300개 이상의 암 모델에서 거의 2만개 가까운 유전자를 정지시켜 암 생존에 결정적인 역할을 하는 유전자를 밝혀냈다. 이 유전자에 작용하는 약물을 개발해 투여하면 암 생존을 저해함으로써 치료 효과를 얻을 수 있다.
연구팀은 폐암과 대장암, 유방암과 같은 일반적인 암과 함께, 새로운 치료법이 긴급하게 필요한 폐암과 난소암 및 췌장암에 관심을 집중했다.
이런 노력의 결과 수천 개의 핵심 암 유전자가 밝혀졌다. 아울러 약물 개발 우선순위 시스템을 개발해 2만여 개 유전자 가운데 신약 개발 가능성이 가장 큰 600개 유전자를 추려냈다.

최상의 타깃을 찾아라
다양한 암 유형 가운데 최고 점수를 얻은 타깃은 베르너 증후군 RecQ 헬리카제(WRN)로 확인됐다. 연구팀은 미소부수체 불안정 암으로 알려진, 잘못된 DNA 수리 경로를 가진 암세포들이 생존을 위해 WRN 효소가 필요하다는 사실을 발견했다.
미소부수체 불안정성(microsatellite instability)은 대장암의 15%와 위암의 28%를 포함해 많은 다양한 암 유형에서 발생하는 것으로 알려져 있다. 이번 연구를 통해 WRN을 유망한 약물 표적으로 새롭게 확인함으로써 WRN을 타깃으로 한 최초의 암 치료제를 개발할 수 있게 됐다.
논문 제1공저자로 웰컴 생어 연구소와 오픈 타깃에서 활동하다 현재 일본 교토대 생명 및 의학 프런티어 연구소에서 근무하고 있는 고스케 유사(Kosuke Yusa) 박사는 “크리스퍼는 5년 전에는 생각할 수 없었던 규모와 정확성으로 과학 연구를 가능케 한 매우 강력한 도구”라며, “이를 통해 암을 표적으로 한 놀라운 신약 개발 기회를 발견했다”고 말했다.
같은 논문 제1공저자인 웰컴 생어 연구소 및 오픈 타깃의 프란체스코 이오리오(Francesco Iorio) 박사는 “신약이 임상시험 최종 단계에서 성공하려면 개발 초기에 가장 뛰어난 최상의 표적을 선택하는 것이 중요하다”며, “항암제 개발을 위한 새로운 치료 표적에 대해 데이터 기반 방식으로는 처음으로 유전체 규모에서의 지침을 제공했다”고 덧붙였다.
정밀 암 치료를 위한 ‘암 의존성 관계 지도’
생어연구소와 EMBL-EBI, GSK, 오픈 타깃 사이의 협력은 이번 연구 결과를 새로운 치료법으로 연결하는 데도 큰 힘이 되고 있다.
또한 연구에서 생성된 데이터세트는 정확힌 암 치료를 위한 상세 규정집인 ‘암 의존성 관계 지도’ 생성의 기초가 된다.
논문 공저자인 생어연구소 및 오픈 타깃의 매튜 가넷(Mathew Garnett) 박사는 “암 의존성 관계 지도는 상이한 암들에 존재하는 모든 약점들을 확인해 내는 커다란 노력으로, 우리는 이 정보를 이용해 차세대 정밀 암 치료 역량을 강화할 수 있다”고 말했다.
영국 암 연구소 수석 과학자인 캐런 부스든(Karen Vousden) 교수는 “이번 연구를 매우 강력하게 만드는 것은 바로 규모”라고 지칭하고, “크리스퍼는 항암제 표적 발견을 가속화하는 독특한 도구로서 이번 연구는 긍정적인 방향으로의 매우 중요한 도약”이라고 평가했다.
그는 “다음 단계는 이번 연구에서 암의 취약점으로 확인된 유전자에 대한 완전 분석 연구가 될 것”이라고 덧붙였다.
- 김병희 객원기자
- hanbit7@gmail.com
- 저작권자 2019-04-11 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터