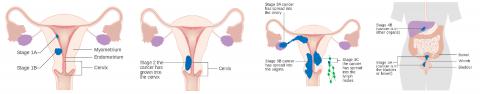
나노입자에 암 치료제를 탑재해 암세포에 주입함으로써 화학요법의 치료 효과를 크게 높일 수 있는 새로운 표적 치료법이 선보였다.
미국 아이오와대 약대 연구팀이 3년 간의 연구 끝에 개발한 이 치료법은 현재 자궁내막암 치료에 성공적인 효과를 나타냈으며, 앞으로 다른 암 치료에도 적용 가능할 것으로 기대되고 있다.
이 치료법은 전통적인 항암 약제와 화학요법에 저항성을 보이는 암세포 공격용 새 약물을 결합해 암세포 침투가 용이한 작은 나노입자에 넣어 주입하는 방식이다. 이 나노입자는 암세포만을 골라 공격하는 극히 선택적이며 암세포에 치명적인 점이 특징. 이번 연구 결과는 과학저널 ‘네이처 나노테크놀러지’(Nature Nanotechnology) 4일자에 보고됐다.
암 표적치료법 개발에 중요한 진전
새 치료법은 2형 자궁내막암 환자의 생존율을 향상시키는 한편, 여러 암의 표적 치료 개발에 중요한 진전을 이룰 것으로 평가되고 있다. 미국에서는 해마다 약6000명의 2형 자궁내막암 새 환자가 발생하는 것으로 집계된다.
현재 시행되고 있는 암치료 표준 화학요법은 전신이 항암 약물에 노출된다는 점이 문제. 이에 비해 표적 치료는 종양 부위에만 직접 약물을 전달함으로써 다른 조직과 기관을 보호하고 약물 효능을 향상시키는 장점이 있다.
논문 제1저자인 카림 이비드(Kareem Ebeid) 대학원생은 “이번의 특별한 연구에서 우리는 암 연구의 가장 큰 난제 중 하나인 암 표적화에 도전했다”며, “처음으로 두 가지 종양 표적화 전략을 결합해 치명적인 2형 자궁내막암 치료에 사용할 수 있었고, 이 치료법은 다른 암에도 적용 가능하다고 믿는다”고 밝혔다.

나노입자가 암 세포 혈관의 구멍 통해 침투
암세포만을 골라 공격하는 치료법을 개발하기 위해 연구팀은 작은 나노입자를 출발점으로 삼았다. 최근에는 나노입자의 크기가 작다는 점 때문에 이를 이용한 암 치료법에 관심이 높아지고 있다. 빠르게 성장하는 암세포가 영양을 공급받기 위해 만드는 혈관은 결함이 있는데다 구멍이 많다. 나노입자는 이 구멍들을 통과할 수 있기 때문에 종양만을 골라 표적화할 수 있는 것.
연구팀은 자궁내막암 치료제인 파클리탁셀과 종양 혈관 성장을 제한하는 비교적 새로운 약물인 닌테다닙(nintedanib) 또는 BIBF 1120 등 두 종의 항암제를 나노입자에 탑재했다. 그러나 이번 연구에서 약물은 다른 용도로도 사용됐다. 닌테다닙은 혈관 성장을 억제하는 것 이외에도 종양세포를 목표로 특정한 돌연변이를 일으켰다. ‘p53 기능 상실’(Loss of Function p53)로 알려진 이 돌연변이는 종양세포의 정상적인 생활주기를 방해하고 화학요법의 치사 효과에 더욱 큰 내성을 갖게 한다.
세포 분열 유도해 살해하는 ‘합성 치사’
화학요법은 세포가 유사분열 등을 포함해 분열할 때 이들을 살해하고, ‘p53 기능 상실’을 일으킨 종양세포들은 종종 이 과정을 지연시키는 유보적 림보(limbo) 상태에 머물러 있게 된다. 이같이 화학요법에 내성을 보이는 암은 치료하기가 훨씬 어렵고 결과도 좋지 않다.
닌테다닙은 종양세포를 공격해 p53 기능 상실을 일으키고 이 세포들이 유사분열 및 세포 분열 상태로 들어가도록 해 이때 화학요법으로 암세포들을 더욱 쉽게 살해할 수 있다. 이비드 연구원은 닌테다딥으로 종양세포가 유사분열 상태로 들어가도록 해 죽이는 ‘합성 치사’(synthetic lethality) 현상을 나타낸 것은 이번 연구가 처음이라고 말했다.
그는 “기본적으로 우리는 종양세포의 아킬레스 건인 p53 기능 상실 돌연변이를 일으킨 다음 쫓아들어가 화학요법으로 암세포들을 괴멸시킨다”며, “대량 세포 사멸 조건을 창출해 내기 때문에 우리는 이것을 종합적 살해 상황이라고 부른다”고 설명했다.

환자 치료 곧 시작
이 같은 세포 사멸 치료법은 p53 기능 상실 돌연변이가 포함되는 자궁암이나 폐암 형태의 암을 포함해 다른 암들의 치료에도 사용될 수 있다.
논문 교신저자인 알리애스거 살렘 아이오와대 약학과 교수는 “이번 연구는 자궁내막암 치료 이외에 더 큰 영향을 미칠 것으로 본다”며, “연구에 사용된 약물이 이미 임상 용도로 승인된 것이므로 곧 환자 치료도 시작할 수 있을 것”이라고 말했다.
에스트로겐 호르몬으로 지탱되는 1형 자궁내막암은 매년 새로 발견되는 자궁내막암의 80%를 차지하는데 비해 2형 자궁내막암은 10~20%로 집계된다. 그러나 2형 자궁내막암이 훨씬 공격적이어서 사망자의 39%를 차지하는 것으로 알려진다.
아이오와의대 산부인과 주임교수인 킴벌리 레슬리(Kimberly K. Leslie) 교수는 “지난 20년 동안 2형 자궁내막암의 표준치료법은 화학요법과 방사선요법이었다”며, “새 치료법은 고도의 표적 선택과 높은 치료 효과로 놀랄 만한 가능성을 보여준다”고 말했다.
- 김병희 객원기자
- hanbit7@gmail.com
- 저작권자 2017-12-05 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터