땅 속에 사는 선형동물과 포유류에서 수명과 건강을 조절하는 새로운 분자 경로가 발견됐다.
미국 케이스웨스턴리저브(CWRU)대 의대 및 병원 연구진은 특정 단백질을 과도하게 갖고 있는 선형동물들이 정상 수치의 단백질을 지닌 것들보다 더 오래 그리고 더 건강하게 산다는 사실을 밝혀냈다. 이와 함께 이들 단백질을 과도한 수준으로 가지고 있는 실험용 쥐들에서 노화와 관련된 혈관 장애가 지연된다는 사실을 입증했다.
과학저널 ‘네이처 커뮤니케이션즈(Nature Communications) 13일자에 발표된 이번 연구는 노화 및 노화 관련 장애를 이해하는데 중요한 영향을 미칠 것으로 보인다. 지금까지는 노화와 관련해 적게 먹을수록 오래 산다는 쥐 실험 연구가 널리 알려져 있었다.
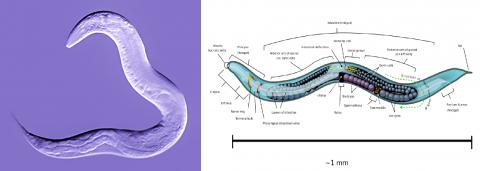
KLF 단백질군이 노화와 수명에 영향 미쳐
논문 제1저자인 CWRU 펠로우 넬슨 시에(Nelson Hsieh) 박사는 “예쁜꼬마선충(Caenorhabditis elegans)을 대상으로 크루펠 유사 전사인자(Kruppel-like transcription factors, KLFs)라는 단백질군의 수치를 늘리거나 줄임으로써 실제로 이 벌레들의 수명을 길거나 짧게 조절할 수 있었다”고 밝혔다. 그는 “정말로 흥미로운 점은 같은 KLF 단백질군이 포유류에도 존재하기 때문에 이 단백질군이 사람 같은 포유류의 노화에 대해서도 유사한 효과를 나타낸다는 점”이라고 강조했다.
논문의 시니어 저자인 무케쉬 제인(Mukesh K. Jain) 교수는 “혈관 기능 이상이 고혈압이나 심장질환, 치매 같은 다양한 노화 관련 질환에 중요한 영향을 미친다는 점을 고려하면, KLF 수치가 연령에 따라 감소하고 이 수치가 줄지 않도록 유지할 경우 노화 관련 혈관질환을 예방할 수 있다는 관찰 연구는 매우 흥미롭다”고 덧붙였다.
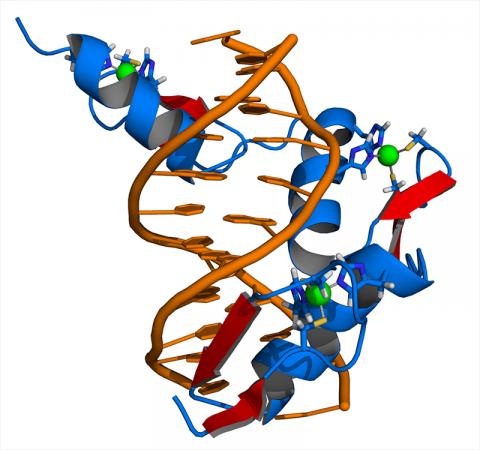
“오토파지 기능으로 노화예방 품질관리”
연구팀은 추가 연구에서 KLF 단백질이 오토파지(autophagy)라는 자가소화작용 조절을 통해 작용한다는 사실을 발견했다. 오토파지는 세포가 잘못 접혀진 단백질이나 노화에 따라 쌓이는 정상적인 분자적 부산물 같은 찌꺼기를 청소하는 일종의 재활용과정이다. 이 같은 품질관리 메커니즘은 통상 노화에 따라 손상돼 간다.
저자들은 “세포가 노화하면서 이 같은 기능을 수행하는 능력도 떨어지게 된다”며, “이렇게 되면 독성 단백질 집합체가 통제할 수 없을 만큼 많이 쌓이면서 궁극적으로 세포 생존을 위협한다”고 설명했다. 실제로 KLF 단백질이 없는 벌레들은 오토파지 기능을 유지하지 못 하고 일찍 죽었다.
“인체에 적용할 방법 연구 예정”
연구팀은 다음 단계로 혈관 안쪽을 둘러싸고 있는 세포들의 오토파지 기능이 혈관 기능 향상에 어떻게 기여하는지 그 정확한 기전을 파악하기 위한 연구를 수행할 계획이다. 아울러 인체에서 KLF 단백질을 표적으로 노화를 조절하는 전략도 모색할 예정이다.
시에 박사는 “우리의 심장과 동맥은 평생 동안 완벽하게 기능해야 하기 때문에 나이가 들어가면서 이 심장과 동맥에 무슨 일이 일어나는지 이해할 필요가 있다”며, “이번 연구 결과는 노화과정 중에 일어날 수 있는 일을 밝혀주는 동시에 이러한 과정을 늦추는 방법을 고안하는 기초를 제공한다”고 말했다.
- 김병희 객원기자
- kna@live.co.kr
- 저작권자 2017-10-16 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터


















