국내 연구진이 간암 세포를 말 그대로 굶겨 죽이는 방법을 학계에 제시했다.
한국연구재단은 서울대 이정원 교수·이화여대 최선 교수 연구팀이 간암 세포 생존을 위해 필수적인 아미노산(아르지닌)을 감지하고 이동능력을 차단하는 기술을 내놨다고 5일 밝혔다.
성과를 담은 논문은 이날 세포 대사 분야 국제학술지 '셀 메타볼리즘'(Cell Metabolism)에 실렸다.
최근 임상 연구에 따르면 간암 세포는 아미노산 중 하나인 아르지닌을 스스로 생성하지 못한다.
아르지닌은 간암 세포 증식과 생존에 절대적으로 필요한 아미노산의 하나다.
보통 외부에서 섭취한다.
아르지닌 분해 효소를 처리해 간암 세포가 아르지닌을 이용할 수 없게 하는 시도가 있었지만, 내성 동반이라는 한계에 부딪혔다.
연구팀은 아르지닌 분해보다는 이동길 차단법을 고안했다.
단백질 합성에 활용되지 않도록 세포질로의 이동을 제한하는 게 성과의 핵심이다.
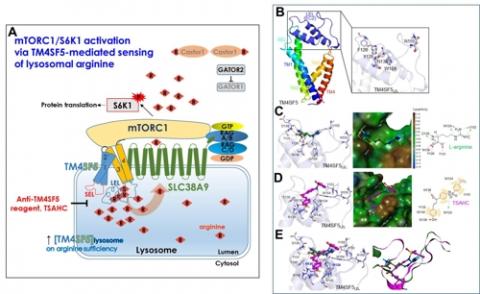
생리적 농도 수준의 아르지닌을 감지하고 이동하도록 하는 요인이 'TM4SF5' 막 단백질인 만큼 그 저해제를 이용했다.
간암 세포가 자식작용(自食作用)을 통해 생체물질을 분해하면 세포소기관(리소좀) 안에 아르지닌이 생긴다.
자식작용은 세포 내 노폐물을 청소하고 박테리아나 바이러스 등 외부 침입자를 제거해 세포 항상성을 유지하는 과정이다.
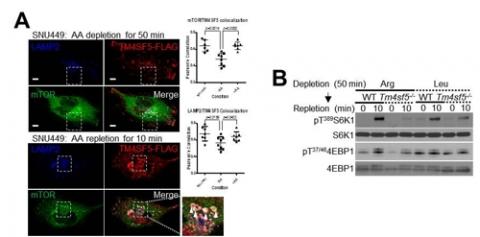
아르지닌 농도가 높을 때 'TM4SF5'는 이를 감지해 세포막에서 리소좀 막으로 이동한다.
이어 아르지닌과 결합해 아르지닌 운송자(SLC38A9)에게 전달한다.
이때 TM4SF5와 함께 리소좀 막으로 이동한 신호전달인자(mTOR)와 단백질 합성에 중요한 하위인자(S6K1) 활성화가 함께 일어난다.
결과적으로 세포질로 옮겨간 아르지닌은 간암세포 생존과 증식에 활용된다.
전체 과정을 복기할 때 TM4SF5 억제 화합물(TSAHC)을 이용하면 TM4SF5와 아르지닌 결합을 억제하고 단백질 합성 신호전달을 저해할 수 있다고 연구팀은 강조했다.
세포 내 아미노산 센서 연구는 미국 매사추세츠공대(MIT) 데이비드 사바티니 박사 연구팀이 독주했다.
이번 연구결과는 그간의 내용을 한발 앞선 것으로 학계에선 평가하고 있다.
이정원 교수는 "그간 정확하게 밝혀지지 않았던 리소좀 내부 아르지닌 감지 센서를 생리적 수준에서 살핀 것"이라며 "아르지닌의 이동성 제어를 통해 궁극적으로 간암 세포를 굶겨 죽일 수 있는 단서를 확인했다"고 말했다.
연구는 과학기술정보통신부·한국연구재단 기초연구사업과 글로벌프런티어 사업 지원으로 수행했다.
- 연합뉴스
- 저작권자 2019-04-05 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터