신종 코로나바이러스(SARS CoV-2) 표면에 돌출된 스파이크 단백질은 이 전염병이 면역 장벽을 뛰어넘어 세계적 대유행을 이끄는 정복자의 창날과 같다.
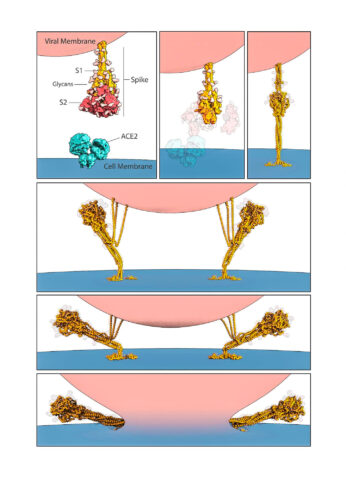
스파이크 단백질은 ACE2 수용체를 통해 인체 세포와 결합한 뒤 극적으로 모양을 변화시킨 다음, 인체 세포막과 바이러스 외부 막을 융합해 감염의 문을 여는 잭나이프 역할을 한다.
때문에 ‘코로나 팬데믹’을 종식시키기 위해서는 스파이크 단백질의 정체와 기능을 최대한 정확하게 파악하는 일이 중요하다.
미국 하버드의대 수련병원인 보스턴 아동병원 연구팀이 처음으로 이 스파이크 단백질의 인체 세포 감염 전과 후의 모습을 정지화면으로 포착하는데 성공했다.
과학저널 ‘사이언스’(Science) 21일 자에 발표된 이번 연구에서는 또 스파이크 단백질의 놀라운 기능도 잡아냈다. 이 스파이크 단백질은 현재 인간 항체가 표적으로 삼는 단백질이자 인체 시험 중인 거의 모든 백신에 사용되는 단백질이다.
예기치 않은 특성
하버드의대 소아과 조교수인 빙 첸(Bing Chen) 박사가 이끄는 연구팀은 이 바이러스가 예기치 않은 특성을 갖고 있어 면역시스템을 회피해 오랫동안 생존할 수 있는 것으로 믿고 있다. 아울러 이 특성들이 백신과 치료제 개발에도 영향을 줄 것으로 보고 있다.
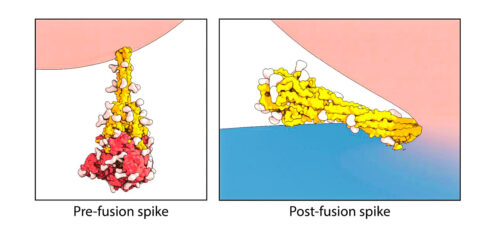
보스턴 아동병원 분자의학부의 첸 박사팀은 극저온 전자현미경(cryogenic electron microscopy) 기술을 사용해 바이러스와 인체 세포막의 융합 전과 후의 스파이크 단백질 구조를 확립했다. 융합 후 스파이크 단백질은 접혀진 단단한 머리핀 모양을 하고 있었다.
연구팀은 또한 바이러스가 흥미롭게도 ACE2 수용체와 결합하지 않았는데도 종종 스파이크 단백질이 원래의 이전 모습에서 융합 이후 모습으로 조기에 모양을 바꾼다는 사실을 발견했다.
첸 박사는 “바이러스가 입체 형태를 바꾸는 두 가지 경로가 있다고 제안한다”며, “하나는 ACE2 수용체에 의존해 바이러스가 숙주세포에 들어갈 수 있도록 하는 것이고, 두 번째는 ACE2와는 독립적인 경로”라고 말했다.
코로나바이러스의 방어 메커니즘?
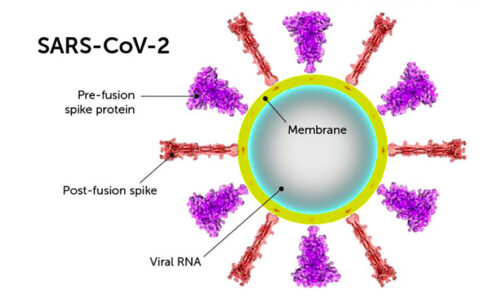
자발적인 형태 변화의 결과로서 코로나바이러스 입자는 종종 바이러스 표면보다 약간 돌출된 단단한 ‘융합 후’의 모습을 지닌, 두 가지 형태의 스파이크 단백질을 지니고 있다.
첸 박사는 SARS CoV-2가 인체 세포와 결합하지 않아도 이런 대체 형태를 취할 수 있는 것은 주위 환경에서의 생존, 예를 들면 표면 위에 떨어져도 부서지지 않도록 하는 방호 역할을 한다고 제안했다.
이는 여러 종류의 물체 표면에서 몇 시간에서 며칠 동안에 걸쳐 생존할 수 있는 이유를 설명해 준다는 것이다.
첸 박사는 “대부분의 바이러스는 숙주 바깥에서 오랫동안 생존하지 못 하는데, 융합 후 SARS CoV-2 스파이크의 이런 견고한 구조가 바이러스를 보호한다고 생각한다”고 밝혔다.
면역 검색을 회피
연구팀은 바이러스가 얼마 간의 스파이크를 가지고 있어 조기에 ‘융합 후 형태’를 취할 수 있는 것은 또한 우리 항체로 하여금 바이러스를 처리 대상으로 삼지 않고 비중화 상태를 유지하도록 유도함으로써 면역계를 회피하는 방법이라고 생각하고 있다.
사실상 융합 후의 스파이크들은 면역계를 혼란시키는 미끼로 작용할 수 있다.
연구팀은 또 융합 전의 스파이크와 비슷한 융합 후의 스파이크들이 표면의 고른 간격이 있는 위치에 당 분자인 글리칸(glycans)을 가지고 있다는 사실을 발견하고 놀랐다. 글리칸은 바이러스가 면역 검색을 피하는데 도움이 되는 또다른 특성이다.
첸 박사는 이번 연구가 백신 개발에 영향을 줄 것이라고 보고 있다. 그는 면역계를 자극하기 위해 스파이크 단백질을 사용하는 현재의 백신 제제는 융합 전후의 형태가 다양하게 혼합될 수 있어 방호 효능에 한계를 나타낼 수 있다고 지적했다.
그는 “스파이크 단백질을 안정화시킬 방법에 대해 생각해야 한다”며, “단백질이 안정적이지 않다면, 비록 항체를 유도해 낼 수는 있지만 바이러스 차단 효과가 떨어질 수 있고, 일괄 처리 변동(batch-to-batch variation)이 있을 수 있다”고 말했다.
HIV 경험을 바탕으로 구축
이번 SARS CoV-2 연구에는 첸 박사가 지난 수년 간 후천성면역결핍증(HIV)을 연구해 온 경험이 큰 도움이 됐다.
두 바이러스 모두 피막 바이러스(envelope viruses)로 알려져 있으며, 세포에 침투하려면 자신들의 외피 막을 숙주 세포의 막과 융합시켜야 한다. 두 바이러스 모두 잭나이프 같은 모양 변경을 하고, 모두 표면에 당이 들어있는 스파이크 단백질을 가지고 있다.
HIV 백신 개발도 중화 항체를 개발해야 하는 어려움에 시달리고 있다. 면역시스템으로 하여금 여러 항체를 생성하도록 혼란을 일으켜 바이러스를 차단하기가 어려운 실정이다.
첸 박사는 “SARS CoV-2는 HIV보다 쉬운 목표물이라고 생각되나 계속 지켜봐야 한다”고 말하고, “이번 1차 백신이 인체 대상으로 안전성과 효능을 확인하는 3상 시험에서 제대로 작동하지 않으면, 이번의 스파이크 구조에 대한 새로운 이해를 활용해 더욱 강력한 백신을 설계하는데 도움을 얻을 수 있을 것”이라고 밝혔다.
- 김병희 객원기자
- hanbit7@gmail.com
- 저작권자 2020-07-22 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터



















