자연살해세포인 'NK세포(Natural Killer Cell)'는 인체 내 면역세포다. 우리 몸속에서 바이러스 감염이나 암세포 같이 형질이 전환된 세포를 특이적으로 인식해 살상하는 역할을 한다.
이러한 공격이 원활히 진행되기 위해서는 ʻ퍼포린(perforin)ʼ 이라는 단백질과 '그랜자임(granzyme)'이라는 단백질이 분비되는 게 필수적이다. NK세포가 암세포를 공격할 때 퍼포린을 분비해 암세포 막에 구멍을 내고 여기에 그랜자임 효소를 넣어 암세포를 사멸시키기 때문이다. 그러나 지금까지 연구된 바에 의하면 활성화되지 않은 NK세포는 세포질 내에 많은 양의 퍼포린 mRNA를 함유하고 있지만 효과인자인 퍼포린 단백질은 상대적으로 매우 낮은 발현을 보이는 것으로 전해진다.
연구에 의하면 NK세포가 활성화 될 때 퍼포린 단백질의 양은 급격하게 증가한다. 학계에서는 이러한 전사 후 조절기작 현상에 대해 '전무장화(prearming)'라는 용어로 설명하고 있는데, 이는 타깃 세포에 대한 면역세포의 급격한 살상반응을 의미한다.
지금까지의 연구는 분자 수준에서의 전사 후 조절기작에 대해 아직 밝히지 못하는 상태였다. 하지만 이러한 전환을 정교하게 이해하는 것은 NK세포의 활성화 기작을 분자수준에서 정확히 설명을 할 수 있기 때문에 매우 중요한 연구로 분류됐다. 관련된 연구는 NK 세포 활성을 조절할 수 있는 타깃 분자를 제시해 항암 면역세포 치료제를 개발하는데 활용할 수 있기 때문이다.
마이크로 RNA ʻmiR-150ʼ 발굴
최근 한국과 미국의 공동연구진이 NK세포 활성 조절에 중요한 영향을 미치는 새로운 '마이크로RNA(mRNA)'를 발굴해 주목받고 있다. 최인표 한국생명공학연구원(이하 생명연) 면역치료제연구센터 박사팀과 그린버그(P. D. Greenberg) 미국 워싱턴대학교 교수팀이 공동으로 연구를 수행했다. 연구는 그 성과를 인정받아 알레르기-면역 분야의 세계적 저널인 '알레르기 및 임상면역학회지(JACI)' 온라인 판에 게재됐다.
학계는 이를 통해 암 및 염증관련 질환과 관련이 있는 것으로 알려진 NK세포 조절을 통한 면역치료제 개발에 기여할 수 있을 것으로 기대하고 있다.
"마이크로RNA(miRNA)는 단백질을 만들지는 않지만 세포의 대사와 증식, 노화, 사멸 등 다양한 생명현상 등에 관여하는 조절인자입니다. 저희 연구팀은 면역세포인 퍼포린 단백질을 조절하는 인자인 새로운 마이크로 RNA인 microRNA-150을 발굴했습니다. 퍼포린은 NK세포가 암세포를 살상하는데 사용하는 단백질이에요. 연구를 통해 새로운 마이크로 RNA(microRNA-150)으로 암을 억제할 수 있었죠."
최인표 박사팀은 실험을 통해 miR-150이 결여된 마우스의 NK세포는 정상 NK세포보다 월등히 높은 퍼포린 단백질이 나타나는 것을 확인했으며, 이와 상응하게 세포 독성은 두 배 이상 높다는 것을 알아냈다. 반면 miR-150을 의도적으로 많이 발현시킨 사람과 마우스의 NK세포는 퍼포린 발현이 저하되며 동시에 세포독성도 저해되는 것을 확인했다.
"이러한 발견은 miR-150이 NK세포의 퍼포린 발현 억제인자로 작용할 뿐 아니라 이와 상응하게 NK세포의 세포독성을 저해하는 중요한 분자라는 것을 규명한 것입니다. 사실 기존의 연구는 퍼포린 단백질을 증가시키는 방법으로 사이토카인 등의 성장인자가 연구 대상이었어요. 하지만 이들은 세포 밖에서 삽입해 줘야 한다는 한계가 있었죠. 저희팀에서 개발한 새로운 마이크로 RNA는 세포 내에 존재하는 인자인 만큼 차별성이 있다고 할 수 있습니다.
"NK활성 극대화 할 수 있다면, 반대도 가능하다 생각했죠"
최인표 박사팀은 miR-150의 역할에 대해 다양한 실험으로 증명을 시도했다. miR-150이 결여된 마우스의 NK세포는 정상 NK세포보다 월등히 높은 퍼포린 단백질을 발현하고 있으며, 이와 상응하게 세포독성도 두 배 이상 높다는 것을 세포독성 에세이와 라이브 이미징(live imaging) 결과분석을 통해 확인했다.
실제로 퍼포린 mRNA에 miR-150 결합부위가 존재하며, 실질적으로 번역 저해를 하는지 확인하기 위해 연구팀은 시험관 내 리포트 에세이(reporter assay)를 수행했다. 그 결과 인간과 마우스의 퍼포린 mRNA는 miR-150의 결합부위가 존재한다는 것을 제시할 수 있었다. miR-150이 결여된 마우스의 NK세포와 달리 miR-150을 과발현시킨 인간과 마우스의 NK세포는 퍼포린의 발현이 저하되고 동시에 세포독성도 저해되는 것을 실험을 통해 확인했다.
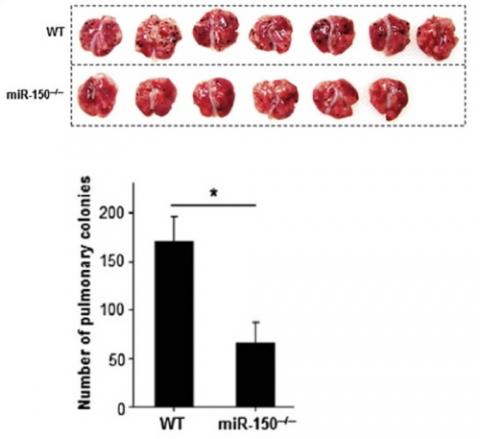
"NK세포의 세포독성에 중요한 조절인자인 miR-150이 동물실험에서도 그 효능을 나타내는지 검증한 결과, 흑색종양의 증식과 전이가 miR-150이 결여된 NK세포를 처리한 군에서 급격히 감소하는 것을 확인했어요."
실험에 실험을 거듭해 진행한 연구. 최인표 박사팀이 이번 연구를 진행한 것은 역발상에 있었다. NK세포 활성을 극대화 할 수 있는 방법이 있다면 암세포를 더 죽일 수 있는 방법 역시 있을 것이라고 생각한 것이다. 그러던 중 새로운 방법으로서 세포 내에 존재하는 마이크로 RNA에 관심을 갖고 접근하기 시작했다.
"사실 마이크로 RNA에 관한 연구는 여러 실험실에 진행되고 있었습니다. 저희 연구는 그 중 하나였던 거죠. 그러던 어느 날 저희팀이 연구를 진행하고 있는 와중에 미국의 한 연구실에서 해당 마이크로 RNA가 NK 분화에 중요한 역할을 한다는 보고를 했습니다. 저희 연구와 유사점도 있었지만 저희팀은 활성에 관한 연구를 하고 있었기 때문에 결국 서로 보완하는 결과를 제출할 수 있던 셈이죠."
최인표 박사팀의 이번 연구는 퍼포린 단백질을 가장 직접적으로 조절하는 인자를 알아내고 그 기능을 생쥐모델에서 규명했다는 데 의의가 있는 것으로 평가받고 있다. 더불어 암세포를 치료할 수 있는 새로운 마이크로 RNA를 발굴하고 실제 암억제 효과를 증명한 것 역시 이번 연구의 가장 큰 의미로 받아들여진다.
"앞으로 현재 기술로 치료가 불가능한 암세포에 대한 치료가 요구될 거예요. 그러기 위해서는 새로운 치료기술이 개발돼야겠죠. 아직 치료가 어려운 난치성 암이 너무나 많습니다. 이런 환자들에게는 새로운 기술 개발이 시급합니다. 이번과 같은 연구결과가 속히 현장에 적용될 수 있도록 여러 가지의 지원책이 있었으면 합니다. 현장에 더욱 적용될 수 있는 좋은 치료기술을 개발하는 것이 앞으로의 바람입니다."
- 황정은 객원기자
- hjuun@naver.com
- 저작권자 2014-06-05 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터